Поле - кристаллизация
Cтраница 1
Поле кристаллизации ( NH4) 2SO4 лежит в области составов систем, содержащих небольшие количества серной кислоты - а Е - с при 10 С и а2Е2с при 90 С. В процессе нейтрализации реакционная масса имеет высокую температуру, но при последующем отделении кристаллов она охлаждается, и это необходимо учитывать при выборе состава реакционного раствора. Практически кислотность раствора поддерживают на уровне 4 - 12 % свободной H2SO4, распределяя серную кислоту в значительном количестве циркулирующего реакционного раствора. [1]
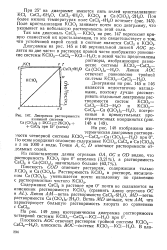 |
Диаграмма растворимости. [2] |
Поле кристаллизации КСЮ3 занимает почти всю диаграмму, что указывает на небольшую растворимость этой соли. [3]
Поле кристаллизации СаСгО4 с повышением температуры увеличивается и при 95 С занимает 97 % всей поверхности диаграммы. [4]
Поле кристаллизации инконгруэнтно плавящегося тройного соединения, как и конгруэнтно плавящегося, на диаграмме плавкости ограничено линиями моновариантных равновесий, отвечающих сосуществованию данного соединения с чистыми компонентами А, В и С. Эти линии двойных выделений пересекаются в трех нонвариантных точках с линиями двойных эвтектик чистых компонентов. Типы диаграмм плавкости с инконгруэнтно плавящимися соединениями тройного состава различаются расположением нонвариантных точек. Известны три разновидности диаграмм плавкости такого типа. [5]
Поле кристаллизации СаН4 ( РО4) - Н2О с повышением температуры сужается и перемещается в область более высоких концентраций кислот, а область Са ( Н2Р04) 2 немного расширяется. Поле кристаллизации Ca ( NO3) 2 - 4H2O при 25 С значительное и исчезает при 50 С. [6]
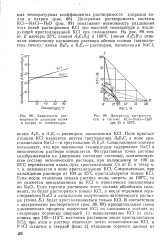 |
Зависимость растворимости хлоридов калия и натрия от температуры.| Диаграмма растворимости в системе КС. - NaCl - Н2О при 25 и ЮО С. [7] |
Поле кристаллизации КС1 находится внутри треугольника А2Е2С, а поле кристаллизации NaCl - в треугольнике B E D. Сопоставление изотерм показывает, что при понижении температуры содержание NaCl в эвтоническом растворе повышается. [8]
 |
Растворимость кремнефторида и фосфатов кальция в водных растворах фосфорной кислоты. Изотерма 60 С. [9] |
Поле кристаллизации монокальцийфосфата соответственно укорачивается, а растворимость его меняется незначительно. [10]
 |
Политерма растворимости системы. [11] |
Поле кристаллизации NaCl при 100 С расширяется, а поле KNO3 - уменьшается с повышением температуры. Отсюда следует, что кристаллизацию NaCl лучше проводить при высоких температурах, a KNOs - при низких. [12]
 |
Прибор для центрифугирования растворов. [13] |
Поле кристаллизации одноводного кислого сульфата занимает значительную область на диаграмме, поэтому соответствующая ветвь изотермы нами изучена более подробно. При более высоких концентрациях серной кислоты Д Анс провел тщательное исследование, и в этой части нами было изучено только несколько точек для того, чтобы установить состав твердых фаз. Полученный цифровой материал приведен в табл. 1 и представлен на рис. 2 в весовых процентах. [14]
 |
Клинографическая проекция. [15] |
Страницы: 1 2 3 4 5