Поле - кристаллизация
Cтраница 2
Поле кристаллизации кристаллогидрата ВР РР2 примыкает к вершине В. [16]
 |
Растворимость тиосульфата аммония в воде.| Растворимость тиосульфата аммония в аммиачной воде при 25 С. [17] |
Поле кристаллизации сульфата аммония занимает основную часть диаграммы и значительно превосходит поле кристаллизации тиосульфата аммония. Это означает, что при выпарке сульфат-тиосульфатной смеси значительная часть сульфата может быть отделена от раствора. Тиосульфат в чистом виде может быть получен лишь в незначительном количестве. Таким образом, анализ системы ( NH4) 2SO4 - ( NH4) 2S2O3 - H2O показывает, что фракционированная кристаллизация сульфат-тиосульфатных смесей экономически нецелесообразна. [18]
 |
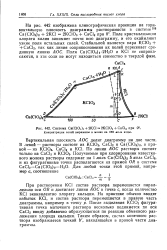
Трехкомпонентная система СаО - А12О3 - SiOa. [19] |
Поле кристаллизации двухкальциевого силиката ( C2S) занимает большую площадь. [20]
 |
Система Са ( СЮ3 2 2КС1 2КСЮ3 CaClj при 0. Концентрации солей выражены в молах на 1000 моль воды. [21] |
Поле кристаллизации хлората калия занимает почти всю диаграмму, и его окаймляют узкие поля остальных солей. Стабильной является пара КСЮз СаС1г, так как линия соприкосновения их полей пересекает срединную линию АОС. [22]
Поле кристаллизации хлорида калия, занимающее 5 30 % площади квадрата диаграммы, вытянуто узкой полосой вдоль боковой стороны хлоридов калия и лития. Ограниченное точками I, VI, VII, VIII и II, оно соприкасается с остальными четырьмя полями диаграммы. [23]
Поле кристаллизации твердого раствора на основе меди имеет значительное протяжение. Оно обладает сложной складкой несингулярного типа, отвечающей псевдобинарному разрезу Си-CuMgZn, и, кроме того, в области больших содержаний цинка еще одной, более слабо выраженной складкой. [24]
 |
Политерма системы Na, Mg Cl, S04 - Н20 в области температур выше 5 С.| Изотерма 0 С взаимно-обратимой системы КШ, К Н2Р04, Cl-HtO. [25] |
Поле кристаллизации твердых растворов NH4H2P04 - КН2Р04 характеризуется вогнутостью, берущей начало в минимальной точке системы NH4H2P04 - КН2Р04 - Н2О и направляющейся к тройной эвтонической точке совместной кристаллизации трех твердых фаз. По мере приближения к тройной эвтонической точке изгиб изогидр постепенно уменьшается. [26]
 |
Центральная проекция изотермы простой четверной системы в случае, когда одна из солей ( В образует кристаллогидрат. [27] |
Поле кристаллизации кристаллогидрата ВР РР примыкает к вершине В. [28]
Поле кристаллизации моногидрата сульфата лития тоже небольшое по площади ( 6 25 %) и узкое - вытянуто вдоль линии состава литиевых солей. Такая форма поля объясняется, с одной стороны, высаливающим эффектом хлоридов, в особенности хлорида лития, а с другой - реакционной способностью сульфата лития образовывать с двойной солью твердые растворы. Поле кристаллизации моногидрата сульфата лития, как и поле Li2SO4 K2SO4, по мере увеличения концентрации хлоридов постепенно расширяется, что указывает на уменьшение растворимости сульфатных солей в присутствии хлоридов. [29]
Поле кристаллизации моногидрата хлорида лития граничит с полями хлорида калия и моногидрата сульфата лития - оно очень маленькое, составляет лишь 0 03 % всей площади, что указывает на высокую растворимость хлорида лития. [30]
Страницы: 1 2 3 4 5