Первый закон - термодинамика
Cтраница 1
Первый закон термодинамики - это частный случай закона сохранения и превращения энергии применительно к тепловым процессам. Согласно этому закону при тепловых процессах теплота может переходить в работу, а работа - в теплоту, причем этот переход осуществляется в строго эквивалентных количествах. [1]
Первый закон термодинамики формулируется по-разному. Одна формулировка выражается соотношением эквивалентности А JQ. [2]
Первый закон термодинамики является законом сохранения и превращения энергии в применении к тем процессам, которые сопровождаются выделением, поглощением или преобразованием теплоты. [3]
Первый закон термодинамики является основой при расчетах энергетического баланса процесса и, в частности, служит для подсчета тепловых эффектов химических реакций. [4]
Первый закон термодинамики устанавливает эквивалентность при превращении различных форм энергии из одного вида в другой, но не дает никаких указаний о возможности и направлении процессов, при которых могут происходить те или иные превращения энергии. [5]
Первый закон термодинамики применим и к биологическим системам, например к живым организмам, в которых протекают биохимические, физиологические и другие процессы, сопровождающиеся превращением энергии. Изучение обмена веществ, в частности ассимиляции и диссимиляции, измерения всего выделяемого человеком тепла, поглощенного им кислорода, выдыхаемых двуокиси углерода и азота, выделяемой мочи и др., вычисление полного баланса метаболизма белков, жиров и углеводов позволило показать, что пищевые продукты при окислении в организме высвобождают такое же количество энергии, как при сжигании их до тех же конечных веществ вне организма. Энергетический баланс процессов подчиняется первому закону термодинамики. В процессе обмена веществ организм принимает из внешней среды разнообразные вещества. Они в организме подвергаются глубоким изменениям, в результате которых превращаются в вещества самого организма. Одновременно вещества живого организма разлагаются, выделяя энергию и продукты разложения во внешнюю среду. Специфично для живых тел то, что эти реакции определенным образом организованы во времени, согласованы между собой и образуют целостную систему, обусловливающую единство ассимиляции и диссимиляции и направленную на постоянное самовосстановление и самосохранение живого тела. [6]
Первый закон термодинамики позволяет составить энергетический баланс термодинамического процесса, но не дает никаких указаний о его возможности и направлении. Происходящие в природе и осуществляемые в технологии процессы, как правило, имеют направленность - самопроизвольно совершаются только в одном направлении, хотя первый закон не запрещает их протекание и в обратном направлении. Например, раствор образуется самопроизвольно, но не может сам собой разделиться на составляющие его компоненты. Все реальные процессы протекают так, что со временем достигают конечного состояния, которое обычно называют равновесным. При этом важно решать такие задачи не только качественно, но и овладеть методами количественного расчета равновесий. Как и первый закон, второй закон ( начало) есть результат обобщения многовекового опыта человечества. [7]
Первый закон термодинамики представляет собой сущность закона сохранения энергии. [8]
Первый закон термодинамики устанавливает только соотношения между количествами энергии разных видов при их взаимных превращениях: он ничего не говорит о том, каким путем можно добиться такого превращения и всегда ли это возможно. Эти вопросы решаются вторым законом термодинамики. [9]
Первый закон термодинамики устанавливает взаимозависимость между количеством сообщенного рабочему телу или отведенного от него тепла, величиной изменения его внутренней энергии и совершенной рабочим телом работы изменения объема. [10]
Первый закон термодинамики, выражающий неуничтожимость энергии и устанавливающий эквивалентность различных форм энергии, не дает никаких указаний на то, в каком направлении и до какого предела будет протекать тот или иной процесс, связанный с определенным превращением энергии. Второй закон термодинамики дает возможность установить, какой процесс может протекать в данной системе без сообщения энергии извне, каков предел его протекания и какое количество работы может быть получено при этом. В этом заключается большое теоретическое и практическое значение второго закона. [11]
Первый закон термодинамики позволяет предсказывать изменения в исследуемой системе и окружающей среде, происходящие в результате термодинамических процессов, в отсутствие на самом деле самих процессов. Причем вопрос о возможности реализации рассматриваемого процесса никак не отражается на результатах расчетов. Например, при расчете тепловых эффектов реакций или других энергетических явлений, сопровождающих их, безразлично, происходят ли эти процессы или они - лишь плод воображения. [12]
Первый закон термодинамики дает возможность вычислить внутреннюю энергию системы U с помощью измеряемых на опыте величин, а не через энергии отдельных частиц, которые невозможно определить в макроскопическом эксперименте. [13]
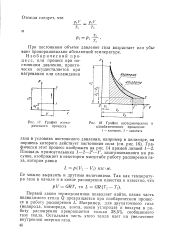 |
График изотермического и адиабатического процессов. 1 - изотерма, 2 - адиабата. [14] |
Первый закон термодинамики позволяет найти, какая часть подводимого тепла Q превращается при изобарическом процессе в работу расширения L. Например, для двухатомного газа ( водорода, кислорода, азота, окиси углерода) и воздуха в работу расширения превращается только 28 5 % сообщаемого газу тепла. Остальная часть этого тепла идет на увеличение внутренней энергии газа. [15]
Страницы: 1 2 3 4