Первый закон - термодинамика
Cтраница 3
Первый закон термодинамики устанавливает, что в общем случае любая система может совершить работу за счет трех источников энергии: внутренней энергии системы, энергии внешней среды, получаемой в форме теплоты, и энергии внешней среды, получаемой в форме работы. Единственным ограничением процесса производства работы при этом является требование, чтобы количество произведенной системой работы точно равнялось сумме убыли внутренней энергии системы и количества энергии внешней среды, переданной системе в форме теплоты и работы. [31]
Первый закон термодинамики выражает собой закон сохранения энергии для замкнутых или для изолированных систем. [32]
Первый закон термодинамики устанавливает эквивалентность различных форм энергии, в частности, внутренней энергии, теплоты и работы. Если система изолирована от окружающего мира, то ее внутренняя энергия остается неизменной. С точки зрения первого закона возможны и равновероятны любые процессы, в которых вместо исчезнувшего одного вида энергии появится эквивалентное количество другого вида. Так, первому закону не противоречило бы поднятие груза или закручивание какой-либо пружины за счет внутренней энергии окружающей среды. Почему, в самом деле, камень, лежащий на земле, не может подняться на какую-то высоту за счет охлаждения окружающего воздуха. [33]
 |
Работа в цикле. выражении ( 76 и алгебраическим зна. [34] |
Первый закон термодинамики рассматривает взаимопревращения тепла и механической работы. По этому закону тепло превращается в механическую работу или, наоборот, механическая работа в тепло в строго эквивалентных количествах. Это означает, что из данного количества тепла при его полном превращении в работу получается определенное количество работы. Точно так же из данного количества работы при ее полном превращении в тепло получается определенное количество тепла. [35]
Первый закон термодинамики устанавливает эквивалентность тепловой и механической энергии и количественную зависимость при их взаимных преобразованиях, но ничего не говорит об условиях этого преобразования. Между тем из опыта известно, что преобразование всех видов энергии в тепловую может происходить без каких-либо ограничений и дополнительных условий. Кроме этого, даже в наивыгоднейшем идеальном цикле Карно в работу может быть превращена только часть тепла, другая часть передается нижнему источнику. [36]
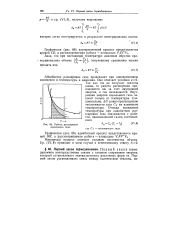 |
Работа расширения идеального газа. [37] |
Первый закон термодинамики непосредственно связан с законом сохранения энергии, который устанавливает эквивалентность различных форм ее. [38]
Первый закон термодинамики справедлив и для обычных систем, состоящих из большого числа частиц, и для систем из небольшого числа частиц, и для отдельных частиц. Второй же закон носит статистический характер и относится исключительно к системам из очень большого числа частиц, так как только к таким системам строго применимы законы статистики. Если же рассматривать системы из не очень большого числа частиц, то выводы из второго закона не могут быть строго применимы к ним. К системам же из малого числа частиц второй закон не относится. [39]
Первый закон термодинамики является формой выражения закона сохранения энергии. Согласно этому закону, энергия не может ни создаваться, ни исчезать, но может превращаться из одной формы в другую. Его справедливость доказана многовековым опытом человечества. [40]
Первый закон термодинамики основан на законе сохранения энергии при взаимопревращениях ее в разных процессах. [41]
Первый закон термодинамики определяет, что подведенная к системе теплота расходуется на увеличение внутренней энергии и производство работы разного типа. [42]
Первый закон термодинамики формулируется в термодинамике координированных систем следующим образом. [43]
Первый закон термодинамики формулируется по-разному. Одна формулировка выражается соотношением эквивалентности А JQ. [44]
Первый закон термодинамики устанавливает, что при взаимных превращениях различных видов энергии переход одного вида энергии в другой совершается в строго эквивалентных количествах. [45]
Страницы: 1 2 3 4