Полимиксин
Cтраница 3
Синтез фрагментов молекулы полимиксина М в основном сводится к получению пептидов диаминомасляной кислоты с треонином, лейцином и ацильных производных с остатком жирно-й кислоты. [31]
С другой стороны, полимиксины обладают способностью активировать фосфолипазы внешней мембраны грамотрицательных бактерий, что также может приводить к разрушению мембраны и гибели микроорганизма. [32]
При наличии флоримицина или полимиксина в виде паров и аэрозолей пробу воздуха отбирают через фильтр, влоЬкенный в патрон и последовательно соединенный поглотитель, заполненный 4 мл дистиллированной воды. [33]
На ранних стадиях исследования полимиксинов были встречены трудности с количественным определением их аминокислотного состава и при выяснении конфигурации входящих в них аминокислот. Эти трудности были связаны в первую очередь с высоким содержанием остатков а у-диаминомасляной кислоты и низким - моноаминокислот. [34]
Для разделения антибиотиков группы полимиксина предложено несколько систем. [35]
Антибиотики - полипептиды - грамицидин, полимиксин и др. По строению они являются циклопептидами из остатков L я D-минокислот. Полимиксин продуцируют Bacillus polymyxa, В. [36]
Одну из таких групп антибиотиков-полипептидов составляют полимиксины, образуемые различными расами Bacillus polymyxa. Они обладают сильной избирательной активностью в отношении некоторых бактерий ( например, синегнойной палочки), очень устойчивых к действию других антибиотиков. Полимиксины имеют главным образом местное применение, так как они оказывают довольно сильное побочное действие на почки. [37]
Наряду с приведенной структурой химическим свойствам полимиксина М могут соответствовать и другие. Однако работами Фоглера, связанными с установлением строения родственного полимиксина BI, внесены известные ограничения. Им показано, что при синтезе октацик-лопептида с дипептидом в боковой цепи биологическая активность убывает на целый порядок, из чего следует, что дипептид в боковой цепи не свойствен природному антибиотику. [38]
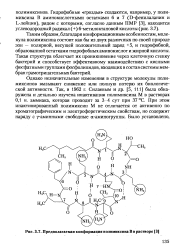 |
Предполагаемая конформация полимиксина В в растворе. [39] |
Однако незначительные изменения в структуре молекулы полимиксинов вызывают снижение или полную потерю их биологической активности. При этом инактивированный полимиксин М не отличается от активного по хроматографическим и электрофоретическим свойствам, но содержит наряду с у-аминными свободные сс-аминогруппы. [40]
Из них наиболее важными являются грамицидины и полимиксины. В последние годы осуществлен синтез грамицидина, благодаря чему уточнен его химический состав и строение. [41]
Из результатов проведенных опытов следует, что полимиксин М, неомицин и мицерин вызывают деформацию альбуминов, а - и р-глобу-линов; гл булины остаются без изменений; мономицин вызывает деформацию только фракции альбуминов. Стрептомицин и дигидростреп-томицин вызывают деформацию так же альбуминов и а - и р-глобули-нов. Фибриноген и у-глобулин со всеми исследованными антибиотиками-основаниями деформации не дают. [42]
Сюда относится, кроме упомянутых грамицидина и полимиксина, альбомицин. [43]
С помощью бумажной и тонкослойной хроматографии были разделены полимиксины Si и T. Электрофоретическая система, описанная для бацитрацина, пригодна и для характеристики полимиксинов. [44]
Таким образом, благодаря конформационным особенностям, молекула полимиксина состоит как бы из двух различных по своей природе зон - полярной, несущей положительный заряд 5, и гидрофобной, образованной остатками гидрофобных аминокислот и жирной кислоты. Такая структура облегчает их проникновение через клеточную стенку бактерий и способствует эффективному взаимодействию с кислыми фосфатными группами фосфолипидов, входящих в состав системы мембран грамотрицательных бактерий. [45]
Страницы: 1 2 3 4