Бургель
Cтраница 1
Бургель в своих исследованиях не применял механического перемешивания, однако последнее необходимо, если реакцию проводят 0 минеральном масле. [1]
Бургель [13] первый применил для реакции алки-лирования ацетилена алкилсульфат, действуя на натриевые производные ал кил ацетиленов диметилсульфа-том в растворе эфира. В реакцию вступает только одна метильная группа, и в качестве побочного продукта образуется натриевая соль метил серной кислоты. Трюше [14] применил аналогичным образом этиловый и бутиловый эфиры р-толуолсульфокислоты и аллиловый эфир бензолсульфокислоты. Авторы этой книги совместно ( с сотрудниками обнаружили возможность получения I метилацетилена и этил ацетилена, с прекрасным выходом. Джон - сон, Шварц и Джэкобс [15] приготовили некоторые ал кил - и хлоралкил ацетилены, действуя эфирами / 7-то-луолсульфокислоты на натриевые и магний-галоидо-производные ацетилена и алкилацетиленов. [2]
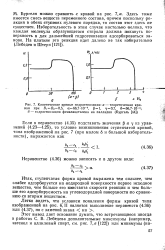 |
Кинетические кривые гидрогенизации. а - теоретическая кривая при В 5, 0 5, а66 7 - 10 - 4, р 1, 0 7, 656 7 - 10 - 5. б - гидрогенизация фенилацетилена на палладии ( Бургель. [3] |
Бургеля можно сравнить с кривой на рис. 7 а. Здесь тоже имеется смесь веществ переменного состава, причем поскольку ре-акция в обеих ступенях нулевого порядка, то состав этот здесь не существен. Избирательность в этом случае настолько велика, что каждая молекула образующегося стирола должна покинуть поверхность и для дальнейшей гидрогенизации адсорбироваться заново. [4]
По данным Бургеля [19], применение при дегало-генировании вместо КОН амида натрия дает возможность избежать изомеризации в диа л кил ацетиленовые углеводороды и расширяет число галоидопроизводных, которые могут быть использованы в синтезе ацетиленовых углеводородов. [5]
В 1929 г. Бургель подробно изучил этот вопрос [14] и пришел к выводу, что сама по себе гидрогенизация вполне стереоспецифична. [6]
Механизм каталитической гидрогенизации Бургелем, Греди, Кустелем и Белисом [10] описывается следующим образом: палладиевый гидрогенизацион-ный катализатор поглощает водород, покрываясь пленкой PdnH2, которая поверхностной группировкой Н - Pd Н обращена к органической фазе; восстанавливаемое вещество адсорбируется на этой пленке той частью молекулы, которая подвергается гидрогенизации, оно может удаляться с нее в активированном состоянии; активная молекула может соединяться с водородом или подвергается деактивации или стереомутации. [7]
Для получения цпклогексилпропнна ( 2) Леспио п Бургель 161 растирали в ступке взятый в избытке продажный А. [8]
Исследуя процессы гидрогенизации ацетилена над палладиевым катализатором на холоду, Бургель [9] предложил различать три фазы в течении реакции: 1) образование комплекса PdnHa; 2) образование нового комплекса PdnH2 - С2Н2 и 3) разложение последнего на палладий и производное этилена, при этом цикл возобновляется. [9]
При применении же амида натрия тройная связь перемещается, согласно Бургелю [1442], даже и из более отдаленных положений к концу цепи. Аналогичное явление наблюдается и при переходе ацетиленовой связи в алленовую; так, например, изопропилаце-тилен превращается, по Фаворскому ( цит. СН - С; СН - ( СН3) 2: С: С: СН2; это же последнее соединение может перегруппироваться при действии металлического натрия в изопро-пилацетиленнатрий, следовательно, обратно в исходный продукт. [10]
При применении же амида натрия тройная связь перемещается, согласно Бургелю [ M42J, даже и из более отдаленных положений к концу цепи. [11]
На рис. 7, б приведена экспериментальная кривая гидрирования фенилацетилена на Pd, полученная Бургелем 44 ] ( ср. [13]
Децин-1 ( СОП, 1, 513; выход 68 %) и циклогексилпропин-3 ( СОП, 1, 511; выход 66 %) получают по методу Леспио - Бургеля ( стр. [14]
Итак, оказалось возможным теоретически вывести кинетическое уравнение гидрогенизации. Бургель [94] пытался решить такую задачу, но вследствие неудачи сделанных попыток пришел к неверному заключению, что гидрогенизация происходит в объеме. [15]
Страницы: 1 2
