Половина - длина - связь
Cтраница 1
Половина длины связи в Н2 равна 0 375, но эту длину нельзя использовать, если Н связан с другими атомами. Значение 0 28 получено вычитанием радиуса X из различных длин Н - Х - связей. [1]
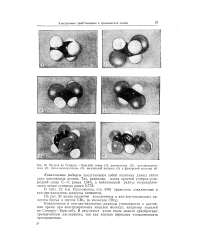 |
Модели по Стюарту - Бриглебу этана ( /, дихлорэтана ( 2, ч с-дихлорэти-лена ( 3, тронс-дихлорэтилена ( 4, малеиновой кислоты ( 5 и фумарояой кислоты ( 6. [2] |
Ковалентные радиусы представляют собой половину длины связи двух одинаковых атомов. Так, например, длина простой углерод-углеродной связи С-С равна 1.54 А, а ковалентный радиус тетраэдри че-ского атома углерода равен 0.77 А. [3]
Радиус пробной сферы равен половине длины связи N-N. Очевидно, что заядерная область создает компоненту силы, направленную так же, как и сила ядерно-ядерного отталкивания, и не может играть связующей роли. Связующую роль играет в этом случае только межъядерная часть электронного облака, которая дает связывающую силу. Эта сила от межъядерной области компенсирует как силу ядерно-ядерного отталкивания, так и антисвязывающую силу от за-ядерных областей. Максимум связывающей силы приходится на середину связи. Таким образом, исследование распределения сил в молекуле N2 дает достаточно очевидный результат: ковалентная связь образуется за счет той части общего электронного облака молекулы, которая сосредоточена между ядрами. [4]
 |
Строение молекул триазида циануровой. [5] |
Гидразин N2H4 исследован электронографически, и половина длины связи N - N принята как ковалентный радиус азота ( см. табл. 6), Структура дифторида гидразина описана на стр. [6]
 |
Полусферические модели атомов ( модели Ciioapia-Брнглеба. [7] |
Ковалентный радиус атома ( г) - это половина длины ковален-тной связи между двумя одинаковыми атомами. [8]
 |
Молекула F2 с ковалснтной связью F-F ( а и гипотетическая ионная молекула F F - ( б.| Расчетные и экспериментальные значения длины / АВ связей в некоторых молекулах. [9] |
В табл. 7.1 приведены значения ковалентных радиусов, рассчитанные как половина длины гомоатомной связи. Во многих случаях измерить длину одинарной гомоатомной связи невозможно, и значение ковалентного радиуса атома элемента А получено вычитанием ковалентного радиуса атома элемента В из длины гетероатомной связи А-В. [10]
Составным частям ковалентного соединения можно приписать ковалентный радиус, равный половине длины связи между одинаковыми атомами. [11]
Наблюдаемое постоянство длин связей позволяет, по Сиджви-ку, пользоваться для расчета их суммами эффективных радиусов атомов, равных половине длины связи между атомами одного и того же элемента. [12]
Ковалентный радиус атома водорода принимается при этом равным 0 322 А с таким расчетом, чтобы ковалентный радиус атома углерода 0 771 А был бы в точности равен половине длины связи С - С в этане. Заметим еще, что Коулсон пользовался ошибочным значением длины связи С - Н в этилене 1 071 А, но это не влияет на основные выводы автора. [13]
 |
Перекрывание двух р-орбиталей, приводящее к образованию я-связи. [14] |
Общая длина ящика L определяется числом атомов Z со средней длиной связи / ( в сопряженных системах 0 140 нм) и составляет L ( Z - f - l) J; с каждого конца цепи добавляется по половине длины связи. [15]
Страницы: 1 2