Положение - заместитель
Cтраница 3
Положение заместителей обозначают греческой буквой, нумеруя атомы по алфавиту, начиная от углеродного атома, соседнего с группой СО. [31]
Положение заместителей также оказывает существенную роль. [32]
Положение заместителей в ряду трансактивности для четырехвалентной платины оказывается несколько иным по сравнению с двухвалентной. [33]
Положение заместителей указывают так, чтобы номера по возможности были меньшими. [34]
Положение заместителей указывается номером атома углерода, к которому они присоединены. [35]
Положение заместителей, введенных в бензольное ядро, зависит от условий реакции и природы катализатора. [36]
Положение заместителей у ненасыщенных альдегидов, кетонов и кар-боновых кислот также весьма существенно. [37]
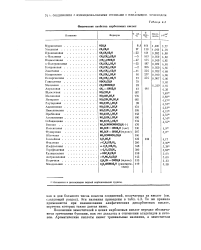 |
Физические свойства карбоновых кислот. [38] |
Положения заместителей в цепях карбоновых кислот нередко обозначаются греческими буквами, как это делалось в отношении альдегидов и кето-нов. [39]
Положение заместителя в молекуле определяет, прежде всего, количество полос поглощения: 9-аминоакридин ( 2) имеет две полосы, 3-аминоакридин ( 3) - три полосы. Положение замещающей группы влияет также на положение максимумов полос. Так, первая полоса поглощения, расположенная в видимой части спектра, у 1-амяноакридина сдвинута в сторону длинных волн по сравнению с ее положением у 3-аминоакридина. У второй полосы аминогруппа в положении 9 вызывает больший батохромный эффект ( стр. Третья полоса, лежащая в ультрафиолетовой области, почти не меняет своего положения при изменении положения заместителя. Заметим, что она чрезвычайно близка по спектральному расположению к соответствующей полосе антрацена. [40]
Положение заместителей обозначают цифрами; если имеются только два заместителя - вместо 1 2 -, 1 3 - и 1 4 - могут быть, соответственно, использованы обозначения о - ( орто -), м - ( мета -) и п - ( пара -), Положение заместителей следует обозначать наименьшими номерами, причем выбор делают согласно правилу А-2, за исключением случаев, когда за основу принимают название одного из соединений, перечисленных в правиле А-12. [41]
Положение заместителей в молекуле определяют обычными методами, прежде всего окислением периодатом. [42]
Положение ядкюгьннтг заместителей при ненасыщенных связях оказывает, в свою очередь, влияние на силы взаимодействия вещества с неполярной фазой. Увеличение объемов удерживания основано на законах, определяющих дипольный момент молекулы. Так, при 25 С гекса-диены-2 4 имеют следующее удерживание ( относительно н-пентана): цис-цис-изомер - 6 13, цис-транс-изомер - 5 7; транс-транс-изомер - 5 16; неподвижная фаза - тетраамилсилан. [43]
Положение заместителей циклогексанов также имеет значение. В порядке повышения детонации идут о -, м - и / г-диметил-циклогексаны с разницей критической степени сжатия, не превышающей одну единицу. Для цис - и яг / жмс-изоме-ров наблюдается заметное и постоянное различие в детонации. Три ifuc - диметилциклогексана слегка выше в детонационном отношении, чем соответствующие транс-изомеры. Эффект раскрытия кольца или сравнение критической степени сжатия циклогексана и н-гексана или н-гексенов аналогичен наблюдаемому для циклопентанов. Циклогексан в детонационном отношении превосходит и-гекеан. [44]
Иногда положение заместителей в насыщенных углеводородных цепях указывают греческими буквами. [45]
Страницы: 1 2 3 4