Положение - химическое равновесие
Cтраница 1
Положение химического равновесия - это достигнутое при равновесии соотношение концентраций реагирующих веществ; оно неизменно для данного состояния химического равновесия. [1]
Положение химического равновесия - достигнутые при равновесии соотношения концентраций реагирующих веществ; оно неизменно для данного химического равновесия. [2]
Положение химического равновесия сохраняется при данных неизменных условиях любое время. При изменении же внешних условий состояние равновесия нарушается, так как при этом скорости противоположных процессов изменяются в разной степени. Однако спустя некоторое время система снова приходит в состояние равновесия, но уже отвечающее новым, изменившимся условиям. [3]
Положение химического равновесия зависит от температуры реакции. Следовательно, температура реакции влияет на все величины, связанные с химическим равновесием. [4]
Положение химического равновесия не зависит от того, с какой стороны оно достигается, со стороны низких или высоких температур. Это состояние не зависит такя: е от механизма и промежуточных этапов химических реакций. В то же время положение равновесия зависит, очевидно, от равновесных значений температуры и давления, так как, по определению, химическое равновесие является динамическим равновесием. [5]
Положение химического равновесия - это достигнутое при равновесии соотношение концентраций реагирующих веществ; оно неизменно для данного состояния химического равновесия. [6]
Расчеты положений химического равновесия получаются гораздо более С10ЖИЫМИ, когда компоненты первоначально смешиваются в произвольных соотношениях и требуется определить равновесный состав. Хороший способ решения таких проблей заключается в составлении таблицы, в которой вертикальные колонки озаглавлены названиями всех участвующих веществ, а в последовательных горизонтальных рядах приведены: 1) начальные количества; 2) изменение одного из компонентов, если оно известно ( иногда это изменение треб ется определить, топа оно обозначается через); 3) изменение количества всех компонентов, которое можно вывести на основании стехиометрии реакции; 4) конечный состав ( вероятно, также выраженный через неизвестное х); 5) мольные до. [7]
Катализатор не сдвигает положения химического равновесия, но ускоряет его достижение. [8]
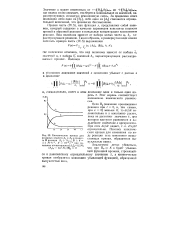 |
Кинетические кривые для исходных веществ А. и Аа и продук-та В реакции А. А2г. В с k 1 М с-1, k Ю-2 с-1 при на-чальных концентрациях [ А1 ] 00 1М. [ AJu - о. 2 М. [ В ] 0 0. [9] |
Этот корень соответствует положению химического равновесия. [10]
Действие различных факторов на положение химического равновесия устанавливается при помощи правила Ле-Ша - телье: если на равновесную систему оказывается внешнее воздействие, то равновесие смещается таким образом, чтобы как можно более ослабить это воздействие. Например, при повышении температуры равновесие смещается в сторону эндотермической реакции; при увеличении давления равновесие сдвигается в сторону образования меньшего числа молекул; при увеличении концентрации реагирующего вещества равновесие смещается в сторону реакции, понижающей концентрацию этого вещества. [11]
Важнейшей величиной в определении положения химического равновесия является константа равновесия, выражающая связь между активностями, концентрациями или парциальными давлениями компонентов реакции в условиях равновесия. [12]
Вместе с тем, поскольку положение химического равновесия той или иной системы, наблюдаемое экспериментально, непосредственно зависит от ее термодинамической характеристики, то значение истинной константы химического равновесия может служить критерием сродства ( точнее, реакционноспособности) обратимо взаимодействующих веществ. Более того, исследуя зависимость константы равновесия от температуры, можно рассчитать все термодинамические константы системы и оценить химическое сродство энергетически. [13]
Постоянная величина К, определяющая положение химического равновесия, называется константой ( равновесия. Эта константа является характерной величиной для каждой обратимой реакции. Следовательно, она различна для различных равновесных обратимых реакций. Таким образом, константой равновесия называется отношение произведения концентраций продуктов прямой реакции к произведению концентраций исходных веществ после достижения равновесия. [14]
Рассмотрим теперь, как влияют на положение химического равновесия концентрации реагирующих компонентов и общее давление. Правая его часть при постоянной температуре есть величина постоянная, поэтому и левая его часть постоянна. Увеличим в нашей газовой смеси парциальное давление одного из компонентов, записанных в уравнении химической реакции ( III. [15]
Страницы: 1 2 3