Положение - сигнал - протон
Cтраница 2
Важно также отметить, что в случае фенилзамещенного пи-ридин - М - имина положение сигналов протонов бензольного кольца по сравнению с сигналами протонов нитробензола и п-нитро-анилина также смещено в сторону сильного поля, что обусловлено увеличением я-электронной плотности и на С-атомах бензольного ядра. [16]
Спектр, как и можно было ожидать, очень сильно упростился. Положение сигналов известных протонов, таких, как протон при С-2 в гистидине, не изменилось, что свидетельствует об отсутствии заметных изменений в характере свернутости полипептидной цепи при замещении большинства протонов на дейтерий. В области резонансных сигналов 5 - СН3 - группы метионина около 8 3т можно ясно различить острые резонансные сигналы четырех остатков Мет, которые в спектре недейтерированного белка скрыты большим числом разных пиков в этой области. [17]
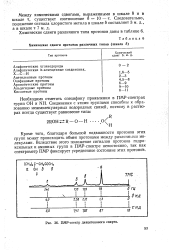 |
Химические сдвиги протонов различных типов ( шкала б.| ПМР-спектр диацетонового спирта. [18] |
Кроме того, благодаря большой подвижности протонов этих групп может происходить обмен протонами между различными молекулами. Вследствие этого положение сигналов протонов гидро-ксильных и аминных групп в ПМР-спектре непостоянно, так как спектрометр ПМР фиксирует усредненное состояние этих протонов. [19]
Было найдено, что положение сигналов протонов алкильных групп и бензольного кольца практически не зависит от концентрации вещества, тогда как сигнал протона гидроксильной группы, как правило, смещается при разбавлении в сторону более высоких полей. Следовательно, изменение положения сигнала протона гидроксильной группы является результатом образования самоассоциа тов. С увеличением объема орто-алкильных заместителей химический сдвиг протона гидроксильной группы в случае неразбавленного раствора возрастает, изменяется и разность химических сдвигов при переходе от разбавленного раствора к неразбавленному. [20]
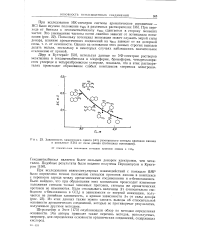 |
Зависимость химического сдвига ( Ат резонансного сигнала протонов хинона в комплексе EDA от силы донора ( потенциал ионизации. [21] |
При исследовании межмолекулярных взаимодействий с помощью ЯМР было определено точное положение сигналов протонов хинона в комплексе с переносом заряда между ароматическими соединениями и я-бензохиноном. Было найдено, что при образовании этих комплексов происходит изменение положения сигнала только хинонных протонов, сигналы же ароматических протонов не изменяются. Из этих данных также можно сделать выводы об относительной основности ароматических соединений, которые не противоречат результатам, полученным другими методами. [22]
Характер связи бутадиен-металл, очевидно, остается тем же. Более того, положение сигналов протонов Ht и Н6 в области исключительно сильных полей указывает на очень сильное экранирование металлом и, следовательно, на очень малую длину связи металл-водород. [23]
О - на - ОО - вызывает смещение положения сигнала протонов с - СН2 - группы на 0 56 млн в сторону слабых полей, для протонов J5 - С - группы - всего О. Данные табл. 4.1.2. [5,10,11] для пероксидов аралкилов и соответствующих непероксид - ных аналогов подтверждают отмеченный характер влияния пероксидной группы. [24]
То обстоятельство, что ( С1СН2) аО является более слабым основанием, чем СН3ОСН2С1, объясняет не только отмеченную выше большую избирательность хлорметилирования, но и отсутствие реакции при использовании 1 моля А1С13 в случае бисхлорметилового эфира: будучи очень слабым основанием, последний неспособен разрушить комплекс А1С13 с карбонильным соединением состава 1: 1, так что реакция не идет из-за отсутствия свободного катализатора. В спектре комплекса 2-ацетотиенона с А1С13 сигналы, всех протонов смещены в сторону слабого поля по сравнению со. В спектре смеси эквимолярных количеств 2-ацетотиенона, СН3ОСН2С1 и А1С13 положение сигналов, отвечающих 2-ацетотиенону, практически совпадает с таковым для образуемого им комплекса, однако сигналы метиленовых и метильных протонов монохлорметилового эфира тоже несколько смещены в слабое поле по сравнению со свободным эфиром. Если же заменить монохлорметиловый эфир бисхлор-метиловым ( образец 8), то положение сигнала протонов ( С1СН2) 2О остается практически тем же, что и у свободного эфира. ПМР-спектр смеси эквимолярных количеств моно -, бисхлорметилового эфира и А1С13 ( образец 9) показывает, что весь хлористый алюминий связан с монохлорметиловым эфиром. [25]
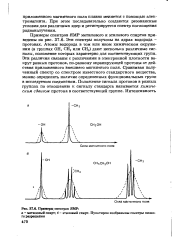 |
Примеры, спектров ЯМР. [26] |
Примеры спектров ЯМР метилового и этилового спиртов приведены на рис. 37.6. Эти спектры получены на ядрах водорода - протонах. Атомы водорода в том или ином химическом окружении ( в группах ОН, СН2 или СН3) дают несколько различные сигналы, положение которых характерно для соответствующих групп. Эти различия связаны с различиями в электронной плотности вокруг разных протонов, по-разному экранирующей протоны от действия приложенного внешнего магнитного поля. Положение сигнала протонов в разных группах по отношению к сигналу стандарта называется химическим сдвигом протона в соответствующей группе. [27]
Степень расщепления компонент дублета определяется шириной линии сигнала, которая в свою очередь обусловливается неоднородностью поля. Для линии 3 дублет наблюдается в том случае, когда VE - vi30 гц. Следовательно, можно рассчитать положения линий 1 и 2, а также химические сдвиги 12сс - и 12р - прото-нов. Следовательно, можно определять положения сигналов протонов А и В в спектре АВХ и проводить конформационный анализ, даже если наблюдается лишь часть X изучаемой системы. [28]
Считают [74], что магнитная анизотропия ароматических соединений вообще не связана непосредственно с делокализацией я-электронов, а целиком обусловлена эффектом локальной анизотропии. Согласно другой точке зрения, разделяемой большим числом исследователей, концепция кольцевых токов правомерна, но неправильно увеличение химического сдвига ароматических протонов целиком относить за счет кольцевого тока. Необходимо учитывать также вклад эффекта локальной анизотропии и влияние распределения электронной плотности. Анализ, проведенный применительно к ароматическим углеводородам [75], показывает, что лишь 50 % или менее от общего увеличения химического сдвига может быть отнесено за счет эффекта делокализации, тогда как остальная часть определяется вкладом локальной анизотропии, особенно значительным для пространственно затрудненных протонов. Влияние электронной плотности на величину химического сдвига иллюстрирует сравнение ПМР-спектров циклооктатетраена ( 13) и его дианиона ( 15): положение сигналов протонов в них почти одинаково, несмотря на то, что дианион ( 15) представляет собой ароматическую частицу, а циклооктатетраен ( 13) - нет. [29]
Страницы: 1 2