Кинетическая закономерность - процесс
Cтраница 1
Кинетические закономерности процессов термической и окисли-тельно деструкции в основном сходны с кинетическими закономерностями цепных реакций окисления и крекинга углеводородов, описанных в гл. [1]
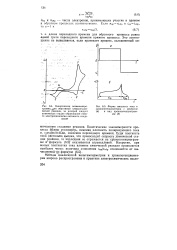 |
Циклическая вольтамперо - rpaMMa. zyiH обратимой электрохимической реакции, за которой следует химическая стадия образования нового электрохимически активного соединения.| Форма импульса тока в. [2] |
Кинетические закономерности процесса йржно установить, изменяя плотность поляризующего тока и, следЬвател ьно, значения переходного времени. [3]
Кинетические закономерности процесса при стационарном состоянии катализатора определяются как кинетикой самой реакции, так и кинетикой изменения поверхности катализатора [11-13], что не позволяет сопоставлять кинетические параметры ( порядки реакции, энергии активации и значения предэкспоненциальных множителей) с характеристиками твердого тела. [4]
Кинетические закономерности процесса и механизм реакции в присутствии ионов железа и меди сходны. [5]
Кинетические закономерности процесса в стационарном состоянии не позволяют, по мнению Белоусова, сопоставлять кинетические параметры с физико-химическими характеристиками твердого тела. В работе [ 1801 была найдена удовлетворительная корреляция между активностью окислов металлов ( определенной импульсным методом) и их термодинамическими свойствами, потенциалом ионизации и радиусом иона катализатора. Оказалось, что наблюдается хорошая корреляция между скоростью восстановления окислов пропиленом и каталитической активностью: чем легче контакт восстанавливается пропиленом, тем он активнее при окислении последнего. Удалось установить прямую связь между валентностью катионов окислов и селективностью окисления углеводородов. В заключение авторы делают существенный, как нам кажется, вывод о том, что для подбора катализаторов целесообразнее вести исследование в импульсных хроматографи-ческих условиях, чем в проточных или циркуляционных. [6]
Кинетические закономерности процессов разделения отражают совокупный результат взаимодействия термодинамических, гидродинамических и геометрических факторов. Поэтому при анализе и проектировании этих процессов в первую очередь должна быть рассмотрена их термодинамика. [7]
Кинетические закономерности процесса восстановления в значительной степени определяются агрегатным состоянием продукта. [8]
Кинетические закономерности процессов абсорбции и ректификации выражаются в большинстве случаев в виде критериальных уравнений. [9]
 |
К составлению материального баланса процесса экстракции. [10] |
Кинетические закономерности процесса экстракции определяются основными законами массопередачи. Поскольку при экстракции происходит массообмен между двумя жидкими фазами, распределяемое вещество переходит из одной жидкости в другую. Для развития поверхности фазового контакта обычно одну из жидкостей диспергируют до капель определенной величины. Таким образом распределяемое вещество переходит из сплошной фазы к поверх. [11]
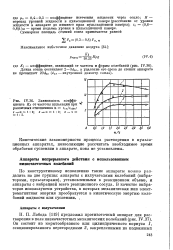 |
Зависимость коэффи -. циента KI от частоты пульсации при различных отношениях а гвх /. цых. [12] |
Кинетические закономерности процесса растворения в пульса-ционных аппаратах, позволяющие рассчитать необходимое время обработки суспензии в аппарате, пока не установлены. [13]
Кинетические закономерности процесса экстракции определяются основными законами массопередачи. Поскольку при экстракции происходит массообмен между двумя жидкими фазами, распределяемое вещество переходит из одной жидкости в другую. Для развития поверхности фазового контакта обычно одну из жидкостей диспергируют до капель определенной величины. Таким образом распределяемое вещество переходит из сплошной фазы к поверхности капли и затем внутрь ее или из капли через поверхность раздела фаз в ядро потока сплошной фазы. [14]
Кинетические закономерности процесса окисления этилена в богатых этиленом смесях свидетельствуют, в частности, о заметном тормозящем действии продуктов реакции. [15]
Страницы: 1 2 3 4