Кинетическая закономерность - реакция
Cтраница 2
Кинетические закономерности реакций окисления фоофина, арсина, сульфана и диоксида серы галогенами, галетами, перекисью водорода и озоном изучали при комнатной температуре в изотермической проточной по газу установке с лотенциометри-ческим устройством. Обнаружено, что по своей активности ркио-лители располагаются в ряд IQjj СГ 2 % Од, а восстановители образуют последовательность: SOg H PE AsHg. Сходство кинетических уравнений указывает на идентичность механизмов этих реакций. [16]
Кинетические закономерности реакций нуклеофильного присоединения, в которых в качестве электрофила выступают трехчленные гетероциклы, такие как пропиленсульфид [44, 45] и этилено-ксид [34, 46-51], во многом отличаются от тех, что характеризуют реакции присоединения к двойной связи. [17]
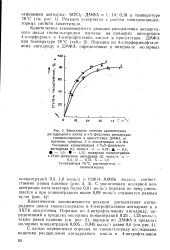 |
Зависимость степени расщепления. ангидридного цикла в 4 - Х - фталевых ангидридах. [18] |
Кинетические закономерности реакции расщепления ангидридного цикла тионилхлоридом в 4-нитрофталевом ангидриде и в АХТК аналогичны. [19]
Кинетические закономерности реакции окисления сульфидов различного строения в присутствии пятиокиси ванадия при температуре ниже 200 С и большом избытке кислорода одинаковы, групповой состав продуктов реакции и пути их образования также сходны, что свидетельствует о близком механизме окисления диметилсульфида и его гомологов. Наблюдаемое на опыте различие в скоростях окисления тиоэфиров ( табл. 119) обусловлено, по-видимому, только различием в строении этих соединений. [20]
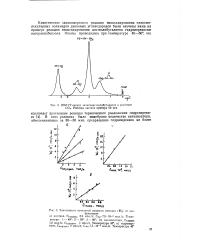 |
ЯМР-Н - спектр эпоксицис-полибутадиена в растворе ССЦ. Рабочая частота прибора 60 мгц.| Зависимость начальной скорости реакции ( 1Р0 от кон. [21] |
Кинетические закономерности реакции зпоксидирования низкомолекулярных полимеров диеновых углеводородов были изучены нами на примере реакции эпоксидирования цис-полибутадиена гидроперекисью изопроиилбензола. [22]
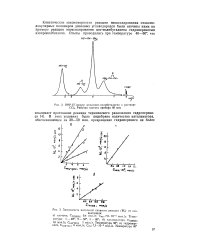 |
ЯМР-Н - спектр эпоксицис-полибутадиена в растворе ССЦ. Рабочая частота прибора 60 мгц.| Зависимость начальной скорости реакции ( W0 от концентрации. [23] |
Кинетические закономерности реакции зпоксидирования низкомолекулярных полимеров диеновых углеводородов были изучены нами на примере реакции зпоксидирования цис-полибутадиена гидроперекисью нзопропилбензола. [24]
Исследованы кинетические закономерности реакции. [25]
Изучены кинетические закономерности реакции и - НДФА и низкомолекулярного цис-полибутадиена. [26]
Исследованы кинетические закономерности реакции. [27]
Исследованы кинетические закономерности реакции ф / счюли-бутадиена с 4 - 1П1трозосоед1шепнямн феполыюго типа, определен второй порядок реакции, предложена схема взаимодействия. [28]
Изучены кинетические закономерности реакции. Найдены частные порядки по всем реагентам. Определена энергия активации реакции, которая составляет 95 95 кДж / моль. [29]
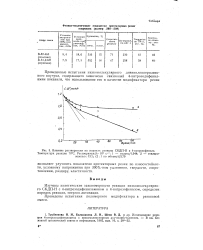 |
Влияние растворителя на скорость реакции СКДП-Н и 4-нитрозофенола. Температура реакции 70 С. Растворитель / k 104 с -. 1 - толуол / 1 944. 2 - этилцел. [30] |
Страницы: 1 2 3 4