Законы - газовое состояние
Cтраница 2
При давлениях газа в городских газовых сетях до 1 МПа ( ГО кгс / см2) законы газового состояния для идеального газа достаточно точно отражают свойства природного газа при изменении его состояния. [16]
При давлениях газа в городских газовых сетях до 1 МПа ( 10 кгс / см2) законы газового состояния для идеального газа достаточно точно отражают свойства природного газа при изменении его состояния. [17]
К важнейшим законам химии относятся закон сохранения массы вещества, закон постоянства состава вещества, закон химических эквивалентов и законы газового состояния. [18]
Квалифицированное ведение технологического режима переработки газа, газового конденсата и нефти требует от оператора знания и умения применять на практике законы газового состояния. [19]
Эта величина характеризует степень отклонения объема реального газа от объема идеального газа. Законы газового состояния ( см. подразд. Реальные газы, особенно при высоких давлениях и низких температурах, имеют значительные отличия от свойств идеального газа. Для того чтобы пользоваться уравнением состояния идеального газа применительно к реальным газам, в него был введен поправочный коэффициент z, который называется коэффициентом сверхсжимаемости. [20]
Законы газового состояния справедливы для идеальных газов. Реальные углеводородные газы также подчиняются этим законам, но с некоторыми отклонениями, зависящими от давления, состава газа и температуры. Природные горючие газы сжимаются сильнее, чем это следует по закону идеального газа. [21]
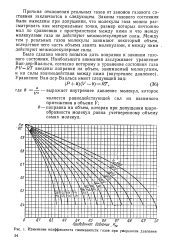 |
Изменение коэффициента сжимаемости газов при умеренном давлении 24. [22] |
Причина отклонения реальных газов от законов газового состояния заключается в следующем. Законы газового состояния были выведены при допущении, что молекулы газа можно рассматривать как материальные точки, размер которых ничтожно мал по сравнению с пространством между ними и что между молекулами газа не действуют межмолекулярные силы. Между тем у реальных газов молекулы занимают некоторый объем, вследствие чего часть объема занята молекулами, и между ними действуют межмолекулярные силы. [23]
Таким образом, при изменении состояния газов параметры его изменяются. Для определения этих изменений выведены специальные законы газового состояния. [24]
К жидкостям неприменимы те же способы исследования, что и к газам или к твердым телам. Исследование дифракции рентгеновских лучей на жидкостях позволяет получить лишь самое общее представление о их строении. К жидкостям неприменимы законы газового состояния, поскольку объем жидкости лишь незначительно изменяется в зависимости от давления и температуры. [25]
Для анализа этих общих законов следует рассматривать открытые системы и возникновение в них динамических структур. Очень важно, чтобы условия, налагаемые на систему, не были бы вполне произвольными. Иначе искомые законы можно проглядеть, подобно тому как исследователь, которому известны лишь свойства тугоплавких металлов при низких температурах, почти наверное проглядел бы законы газового состояния. [26]
Страницы: 1 2