Законы - термодинамика
Cтраница 1
Законы термодинамики указывают на вероятность протекания тех или иных реакций в определенных условиях и устанавливают предельно-достижимые выходы конечных продуктов. [1]
Законы термодинамики не являются следствием каких-то гипотез о строении материи и механизме передачи энергии. [2]
Законы термодинамики, определенные эмпирически, выражают приблизительное и вероятное поведение систем, состоящих из большого числа частиц или, точнее, они выражают законы механики подобных систем так, как они представляются существам, не обладающим достаточной тонкостью восприятия для того, чтобы оценивать величины порядка тех, которые относятся к отдельным частицам, и не могущим повторять свои опыты настолько часто, чтобы получить какие бы то ни было результаты, кроме наиболее вероятных. Законы статистической механики применимы к консервативным системам с любым числом степеней свободы и являются точными. Это не значит, что эти законы труднее установить, нежели приближенные законы для систем с очень большим числом степеней свободы или для специальных классов таких систем. Скорее верно обратное, так как наше внимание не отвлекается от того, что существенно обусловлено особенностями рассматриваемой системы, и мы не вынуждены удовлетвориться предположением, что эффект величин и обстоятельств, которыми мы пренебрегли, в полученном результате можно будет также не принимать во внимание. Законы термодинамики легко могут быть получены из принципов статистической механики, неполным выражением которых они являются, но сами они являются, пожалуй, несколько слепым проводником в наших поисках этих законов. В этом, вероятно, главная причина медленности развития рациональной термодинамики, контрастирующей с быстрым выводом следствий из ее эмпирических законов. [3]
Законы термодинамики выражают вероятное поведение системы, состоящей из большого числа частиц или законы механики для этих частиц. Пригожий [4], описание на вероятностном уровне содержит дополнительную информацию - на этом уровне мы получаем новое динамическое описание, позволяющее предсказывать будущую эволюцию системы без нарушения эквивалентности индивидуальных и статистических уровней. [4]
 |
Зависимость поверхностного натяжения воды на границе с метаном и природным газом от давления.| Зависимость поверхностного натяжения воды на границе с индивидуальными углеводородами при 323 К. [5] |
Законы термодинамики широко применяют при определении свойств углеводородов: удельной теплоемкости газов и жидкостей; теплоты парообразования; энтальпии, энтропии. [6]
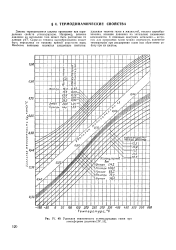 |
Удельная теплоемкость углеводородных газов при атмосферном давлении [ IV. 1В ]. [7] |
Законы термодинамики широко применяют при опре-делении свойств углеводородов. Скрытая теплота парообразоваяия может быть определена по наклону кривой упругости пара. [8]
Законы термодинамики могут формулироваться по-разному. [9]
Законы термодинамики включают в себя общие закономерности, которые характеризуют состояние равновесия системы независимо от каких бы то ни было других факторов. Они могут быть применены к любым мыслимым типам равновесия, как это было показано, например, в разделе 16, для случая равновесия при приложении внешней силы. Эти законы настолько общи, что не зависят от строения химической системы; например, мы знаем, что они применимы к растворам высокомолекулярных соединений, даже если наши представления о структуре таких растворов неполны и могут подвергаться изменению. [10]
Законы термодинамики и различные физико-химические закономерности используют при конструировании реакционных аппаратов, при создании новых технологий и разработке математических моделей для проектирования и управления сложными химико-технологическими комплексами. [11]
Законы термодинамики просты и строги. [12]
 |
Зависимость поверю ост-ного натяжения воды на границе с метаном и природным газом от давления. [13] |
Законы термодинамики широко применяют при определении свойств углеводородов: удельной теплоемкости газов и жидкостей; теплоты парообразования; энтальпии, энтропии. [14]
Законы термодинамики не требуют, чтобы при обратном переходе в исходное состояние равновесия система проходила все те же состояния, в которых она пребывала в процессе вывода из равновесия. [15]
Страницы: 1 2 3 4