Бутилацетилен
Cтраница 3
При этом, так как регулярное возрастание АЯ2 в том же направлении, что и рост электронодонорной способности растворителя маловероятно, наблюдающаяся зависимость между экспериментальной величиной АЯ и электронодонорной способностью растворителя, очевидно, означает определяющую роль Н - связи. Этот вывод подтверждается также систематическим увеличением смещения AVMK и увеличением интегрального коэффициента поглощения полосы vK ( CH) комплекса по сравнению с поглощением мономерного бутилацетилена в этом же растворителе. [31]
При каталитической гидратации ацетилена ( реакция Ку-черова) образуется уксусный альдегид. Какие соединения должны получиться при гидратации следующих гомологов ацетилена: а) метилацетилена, б) этилацетилена, в) метилпропилацетилена, г) диэтилацетилена, д) бутилацетилена, е) этилпропилацетилена. [32]
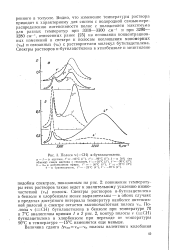 |
Полоса v ( - - СН н-бутилацетилена. [33] |
Спектры растворов н-бутилацетилена в бензоле и хлорбензоле менее выразительны - в обоих случаях в пределах доступного интервала температур наиболее интенсивной полосой в спектре остается высокочастотная полоса VM. Полосы v ( СН) бутилацетилена в бензоле при температуре 70 и 7 С аналогичны кривым 1 и 2 рис. 2, контур полосы v ( CH) бутилацетилена в хлорбензоле при переходе от температуры 90 С к температуре - 15 С изменяется еще меньше. [34]
Промежуточная картина имеет место для остальных исследованных растворителей. В спектрах растворов бутилацетилена в мезити-лене, толуоле и хлорбензоле также обнаружено только по одной полосе. Однако рост полуширины в ряду гексан, хлорбензол, толуол - 12 - - 29 - т - 33 см 1, смещенное положение максимума поглощения для растворов в хлорбензоле и толуоле ( 635 см-1 вместо 629 см-1 для гексана) и явно выраженная асимметрия полосы 629 см - в спектре раствора бутилацетилена в мезитилене с плечом при 645 см 1 - все это указывает на наложение двух полос поглощения свободных бм ( - СН) и связанных бк ( СН) с растворителем молекул бутклацстилсна. [35]
Ссылка заключена в скобки и в ней сообщается: фамилия автора ( авторов) работы, сокращенное название журнала, том и страница. Ссылки эти указывают, что получение бутилацетилена было описано А. Е. Фаворским в статьях, опубликованных в журнале Русского физико-химического общества, часть химическая ( Ж), том 19, стр. [36]
К полученному натриевому производному / npem - бутил ацетилена в эфире прибавляют по каплям, при охлаждении и перемешивании, 42 г свежеперегнанного диметилсульфата. На дне колбы образуется плотный осадок. Эфирный раствор полученного углеводорода сливают с осадка, в котором имеются мельчайшие кусочки непрореагировавшего натрия ( см. примечание 2); осадок несколько раз промывают сухим эфиром. Полученный эфирный раствор 4 4-диметилпентина - 2 ( метил - mpem - бутилацетилена) несколько раз промывают водой, затем 10 % - ным раствором соды, еще раз водой и сушат хлористым кальцием. После отгонки эфира углеводород перегоняют на колонке. [37]
Ряд 1 3 5 - и 1 2 4-тризамещенных бензолов был получен Лутцом [35] в присутствии системы ( С2Н5) 3А1 - TiCh из монозамещенных ацетиленов. Теми же авторами [37] показана возможность совместной циклотримеризации различных ацетиленов. Проведенное Маковецким [39] исследование этой реакции в присутствии ряда каталитических систем на основе соединений титана подтвердило предположение, что активным центром реакции является атом титана. С помощью комплексных катализаторов удалось провести циклотримеризацию некоторых ацетиленов и получить алкилбензолы, что чрезвычайно трудно сделать любыми другими методами. Из-за больших стерическпх затруднений, создаваемых объемными mpem - бутильными группами, предпринимавшиеся ранее попытки провести циклотримеризацию mpem - бутилацетилена на других катализаторах были неудачны. [38]
Страницы: 1 2 3