Вторичный бутилбензол
Cтраница 2
В значительно более поздних работах [244] наблюдалось, что при взаимодействии хлористого бутила с бензолом в присутствии хлористого алюминия всегда образуется вторичный бутилбензол. [16]
В 1951 г. Кац с сотрудниками3, изучая влияние катализатора на состав алкилата при алкилировании бензола этиленом, в диэтилбензольной фракции, получаемой при алкилировании над твердыми катализаторами-алюмосиликаты, твердая фосфорная кислота, фосфат железа - обнаружил вторичный бутилбензол в количестве 5 30 и 41 % соответственно, ал-килирование бензола в присутствии хлористого алюминия при температуре 80 С не сопровождалось этой побочной реакцией. [17]
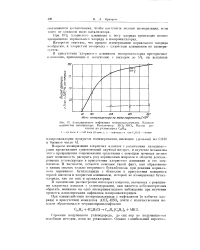 |
Алкшшрованио нафталина пзопропилхлоридом. Влияние количества катализатора. Катализатор A1C12 - HSO4. Выход рассчитан на углеводород С22Н32. [18] |
Вопросы изомеризации хлористых алкилов с различными катализаторами представляют существенный научный интерес. В частности, остается неясным такой факт, как образование в наших опытах только вторичного бутилбензола при реакции нормального первичного бутилхлорида с бензолом в присутствии комплекса серной кислоты и хлористым алюминием, который не изомеризовал бутил-хлорида, так же как и нропилхлорида. [19]
Применение реакции Фриделя-Крафтса для получения алкилбензолов ограничивается тем, что галоидные алкилы, способные к изомеризации, обычно претерпевают это изменение в процессе реакции. Так, например, при применении л-пропиль-ных галоидных производных получаются изопропилбензолы, л-бутильные производные образуют вторичные бутилбензолы, а из изобутильных соединений получаются углеводороды, содержащие третичную бутильную группу. Явления изомеризации мо-тут быть сильно снижены Проведением конденсации при 0 во, но даже и при этих условиях способ этот не пригоден для получения высших нормальных алкилбензолов. [20]
Показано, что содержание крезолов в соответствующих азео-тропах меньше, чем в случае фенола. К тому же в отличие от фенола крезолы вовсе не образуют азеотропов с пропилбензолом и вторичным бутилбензолом, а следовательно, обладают большей селективностью по отношению к компонентам печного масла. Эти обстоятельства ( с учетом достаточной ингибирующей способности крезолов) позволяют сократить расход азеотропного агента и повысить производительность колонн, а также снизить энергетические затраты на ректификацию и расходы на регенерацию добавки. [21]
Применение реакции Фриделя-Крафтса для получения алкилбензолов ограничивается тем, что галоидные алкилы, способные к изомеризации, обычно претерпевают это изменение в процессе реакции. Так, например, при Применении л - пропиль-ных галоидных производных получаются изопропилбензолы, л-бутильные производные образуют вторичные бутилбензолы, а из изобутильных соединений получаются углеводороды, содержащие третичную бутильную группу. Явления изомеризации мо-тут быть сильно снижены проведением конденсации при 0 80, но даже и при этих условиях способ этот не пригоден для получения высших нормальных алкилбензолов. [22]
Общее время реакции при этой температуре должно составлять около 3 час. При более изкой температуре реакция протекает значительно медленнее; при температуре выше - ( - 10 уменьшается выход вторичного бутилбензола. [23]
Здесь при имевшихся концентрациях я - и ж-ксилолы или о-ксилол, стирол и кумол не отделяли один от другого; не происходило также отделение изобутилбензола от вторичного бутилбензола. [24]
Синтетические алкилароматические углеводороды производятся с начала 40 - х годов. Этил - и пропилбензолы идут преимущественно для приготовления стирола, метилстирола и а-метилстирола, являющихся полупродуктами, на основе которых осуществляется производство пластмасс и каучуков. Изопропилбензол и вторичный бутилбензол применяются для производства фенола, ацетона и метилэтилкетона. [25]
Ароматические ннтросоединения обладают селективностью и для более высших ароматических углеводородов. Так, 2 4-динитротрихлорбен-зол, 2 4-динитрохлорбензол, 1 3-динитробензол и пикрат о-нитроанилина удерживают гс-ксилол сильнее, чем изопропилбензол. На пикрате о-нитроанилина вторичный бутилбензол выходит раньше о-ксилола, температура кипения которого на 29 ниже. [26]
Алкилирование бензола бутеном-2 в присутствии кремнефосфорной кислоты ( так называемой твердой фосфорной кислоты) сопровождается структурными изменениями. Так, при 200 - 300 получается от 62 до 75 % бутилбензола, который состоит из смеси вторичного и третичного бутилбензолов. В этом случае вначале протекает изомеризация вторичного бутил-катиона в третичной бутил-ион, а затем бутил-ион конденсируется с бензолом. Только при использовании в качестве катализатора алюмосиликата при 250 получается чистый вторичный бутилбензол. [27]
Видно, что степень диспропорционирования толуола зависит от состава катализатора и условий реакции. Здесь х - мольное отношение Ю2 / А1203, числа перед символом цеолитов указывают степень бмена ионов Na в долях. Эффект зависит от природы катиона. Как видно из табл. 12, при алкилировании бензола этиленом на бифункциональном катализаторе 2 5 % NiO - CaY, который ведет реакцию в направлении образования этилбен-зола и вторичного бутилбензола, соотношение продуктов зависит от условий процесса. В присутствии С03 возрастает выход этилбензола и снижается выход ВББ. Общая же конверсия оле-фина в алкилбензолы та же, что в опытах с азотом. [28]
Страницы: 1 2