Понижение - точка - замерзание
Cтраница 3
Величины осмотического давления, понижения точек замерзания и повышения точек кипения всегда получаются значительно болЫшши, чем вычисленные по формулам. [31]
Для данного растворителя постоянная понижения точки замерзания больше, чем коэффициент повышения температуры кипения ( например, для воды 18 5 С, бензола 51 2 С, камфары 40 С), поэтому этот подход позволяет получить несколько большую чувствительность. [32]
Согласно закону Рауля, понижение точек замерзания или повышение точек кипения не слишком концентрированых растворов в данном растворителе пропорционально. [33]
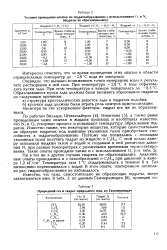 |
Природный газ и гидрат природного газа, по Гаммершмидту. [34] |
Очевидно, это вызвано понижением точки замерзания воды в результате растворения в ней газа. [35]
Следовательног можно сказать, что понижение точки замерзания всех моляльных растворов неэлектролитов в воде является величиной постоянной. Аналогичное наблюдается и для других растворителей. В связи с этим вводится понятие криоскопической константы. [36]
Здесь А Т заы - понижение точки замерзания; А Т кяп - повышение точки кипения; ДР - понижение давления па - ра, фактически наблюдаемое в растворах электролитов, а А7 эам. А РА - значения тех же величин, вычисленные по закону Рауля без учета электролитической диссоциации. [37]
Здесь Д7Г - Т - понижение точки замерзания, 7 - точка замерзания чистого твердого растворителя, а Д - п - i, m - мольная эн-талышя плавления. [38]
Ролла и др. [184] измерили понижение точки замерзания T1NO3 рядом добавок и определили теплоту плавления T1NO3 калориметрически. [39]
Однако вычисленное для этой модели понижение точки замерзания вдвое больше наблюдаемого. Так как координационное число иона Ti4 по отношению к кислородному равно 6, исключая сильно основные системы, естественно допустить, что распределение тетраэдров ТЮ4 среди тетраэдров SiO4 может быть неустойчивым. Если, однако, два иона Ti4 занимают два соседних или очень близко расположенных тетраэдра, координационное число может возрасти за счет образования общих ребер или граней. [40]
Значение ОММ, полученное из понижения точки замерзания, может содержать ошибку, обусловленную рядом причин, в том числе тем, что раствор слишком концентрирован или является нендеа. [41]
Опытным путем установлено, что понижение точки замерзания разбавленного раствора пропорционально концентрации растворенного вещества. В 1883 г, французский химик Ф. М. Рауль сделал очень интересное открытие: понижение точки замерзания, вызываемое различными растворенными веществами, взятыми в одинаковых мольных количествах, одинаково для данного растворителя. [42]
Следовательно, каждой концентрации отвечает определенное понижение точки замерзания раствора сравнительно с точкой замерзания чистой воды. [43]
Совершенно очевидно, что измерение понижения точки замерзания также не может применяться для определения молекулярных весов высокомолекулярных соединений. [44]
Совершенно очевидно, что измерение понижения точки замерзания также не может применяться для определения молекулярных весов белков. [45]
Страницы: 1 2 3 4