Частные порядки
Cтраница 1
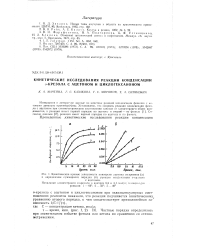 |
Кинетические кривые зависимости конверсии ацетона от времени ( а и определение суммарного порядка ( б реакции конденсации о-крезола. [1] |
Частные порядки определялись при значительном избытке фенола или кетона по сравнению со стехио-метрическим. [2]
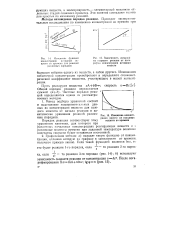 |
Зависимость логарифма скорости реакции от логарифма концентрации исходных веществ. [3] |
Частные порядки реакций определяются одним из рассматриваемых методов. [4]
Частные порядки реакций обычно выражаются целыми числами, редко превышающими двойку. Это справедливо и для реакций, химические уравнения которых имеют большие стехиометрические коэффициенты. [5]
Здесь общий порядок - второй, но частные порядки - дробные. Возможно, это связано с неустойчивостью аминопроизводного. [6]
При кинетических исследованиях обычно подлежат определению константы скорости и частные порядки по реагирующим веществам или кажущийся порядок в эмпирическом уравнении скорости реакции. [7]
На основании результатов экспериментов определялся общин порядок реакции и частные порядки реакции по отдельным реагентам. [8]
Изучена кинетика реакции оксиэтилирования диалкиламинов в присутствии кислотных катализаторов и найдены частные порядки по компонентам. [9]
Изучена кинетика реакции оксиэтилирования диалкиламинов в присутствии кислотных катализаторов и найдены частные порядки по компонентам. Показано, что каталитический эффект пропорционален силе кислоты. [10]
ТБС), так и по ТБС в избытке метанола, что свидетельствует о том, что частные порядки по каждому из исходных спиртов равны первому. [12]
ТБС), так и по ТБС в избытке метанола, что свидетельствует о том, что частные порядки по каждому из исходных спиртов равны первому. [14]
Наиболее подробное изучение кинетики проведено в ДМФ, где варьирование концентраций реагентов показало, что при суммарном втором порядке реакция имеет первые частные порядки. [15]
Страницы: 1 2 3