Порядок - устойчивость
Cтраница 1
Порядок устойчивости к окислению в газовой фазе согласуется с порядком стабильности: метан, этан, изобутан, нормальный бутан, нормальный пентан, изопентан. [1]
Порядок устойчивости в аллилкарбопильпь1х комплексах железа следующий: СО АИ СЬ. [2]
Порядок устойчивости радикалов, таким образом, параллелен порядку устойчивости карбониевых ионов ( ср. [3]
Следует помнить, что порядок устойчивости ряда материалов зависит от состава атмосферы, воздействию которой он подвергается. [4]
Показано также [57], что порядок устойчивости комплексов обусловлен селективностью реагентов по отношению к соответствующим металлам. [5]
Как и в случае карбокатионов, порядок устойчивости свободных радикалов соответствует ряду третичныйвторичный первичный, что также объясняется гиперконъюгацией ( разд. [7]
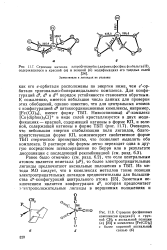 |
Строение катиона хлоро этиленбис ( дифенилфосфин кобальта ( П, содержащегося в красной ( а и зеленой ( б модификациях его твердых солей.| Строение фосфиновых. [8] |
Для конфигураций d8, d9 и d10 порядок устойчивости становится обратным. К сожалению, имеется небольшое число данных для проверки этих обобщений, однако известно, что для центральных атомов с конфигурацией d8 пятикоординационные комплексы, например, [ Fe ( CO) 5 ], имеют форму ТБП. Очевидно, что небольшая энергия стабилизации поля лигандов, благоприятствующая форме КП, компенсирует свойственное форме ТБП стерическое преимущество, что позволяет выделить оба комплекса. В растворе обе формы легко переходят одна в другую посредством псевдоьращения по Берри или в результате диссоциации с последующей рекомбинацией ( см. разд. [9]
Для ионов металлов класса ( а) порядок устойчивости комплексов прямо противоположный. Для комплексов ионов металлов класса ( а) должна существовать хорошая корреляция устойчивости их комплексов с основностью ( по отношению к протону) лигандов. [10]
Из этих данных вытекало что ферроцснилкарбоииевый и трифенилкарбониевый ионы имеют одина ковый порядок устойчивости. [11]
Независимо от способа их генерирования [12] изучение простых алкильных катионов позволило убедительно доказать приведенный выше порядок устойчивости. [12]
В состоянии равновесия найдено примерно 26 % 2 3 4-три - О-метил-в - ксилозы и 70 % 2 3 4-три - 0-метил-в - ликсозы [167], и такой порядок устойчивости является обратным тому, который обычно наблюдают. Эти результаты трудно объяснить; можно лишь представить, что присутствие метоксильных групп в экваториальном поясе благоприятствует аксиальной ориентации, в особенности расположению двух аксиальных групп у соседних углеродных атомов, поскольку в этом случае отсутствует взаимодействие между данными группами. Указанное расположение имеет место в а-формах маннозы и ликсозы. Более ясное понимание этого вопроса может быть достигнуто в результате исследования ( очевидно, еще не завершенного) равновесия между 2 - 0-метилглюкозой и 2 - 0-метилманнозой. [13]
ПО и 112), как показано на рис. 5.33. Следует отметить, что оба типа ангидридов имеют одинаковую циклическую систему диокса-бицикло - [ ЗД1 ] - октана и что для альдогексоз с тало -, галакто - и глкжо-конфигурациями 1 6-ангидрофура-нозы имеют тот же порядок устойчивости, что и соответствующие 1 6-ангидропиранозы. [14]
 |
Система координат для молекул типа А2. [15] |
Страницы: 1 2
