Кажущийся порядок - реакция
Cтраница 1
Кажущийся порядок реакции равен среднему арифметическому между истинным и первым. Названные условия определяют внутридиффузионную область протекания реакции. [1]
Кажущийся порядок реакции падает от единицы до нуля с увеличением покрытия поверхности [ ( аг А) а / ] По-видимому, порядок реакции, близкий к единице, получается также из-за наличия диффузионных эффектов. [2]
Кажущийся порядок реакции, вычисленный по кинетической кривой расходования фурфурола в координатах gc - t, соответствует первому. Следует отметить, что при окислении фурфурола в водной среде уже в начальный период, кроме соединения III, присутствуют продукты дальнейших стадий реакции, и в частности, кислоты. Последние являются катализаторами реакции и, следовательно, найденная константа скорости первой стадии ( / с не является истинной. [3]
Кажущийся порядок реакции по кислороду при РОг Р в обоих случаях близок к нулю. [4]
Кажущийся порядок реакции по веществу А равен минус единице. Такой случай встречается в практике. Например, скорость взаимодействия оксида углерода с кислородом, происходящего на поверхности платинового катализатора, понижается с ростом концентрации оксида углерода. Это объясняется вытеснением молекулами СО молекул О2, вызывающим понижение концентрации адсорбированного кислорода. [5]
Кажущийся порядок реакции по веществу А равен минус единице. Такой случай встречается в практике. Например, скорость взаимодействия оксида углерода с кислородом, происходящего на поверхности платинового катализатора, понижается с ростом концентрации оксида углерода. Это объясняется вытеснением молекулами СО молекул Ог, вызывающим понижение концентрации адсорбированного кислорода. [6]
Кажущийся порядок реакции по водороду, превышающий единицу, указывает на большую сложность течения процесса. Увеличение концентрации водорода не только повышает степень покрытия активных точек каталитической поверхности, но оказывает существенное дополнительное влияние, возможно ускоряя десорбцию цикло-гексана с поверхности катализатора. [7]
Найти кажущийся порядок реакции, исходя из предположения, что скорость реакции определяется скоростью диффузии через уже прореагировавший слой; объяснить, каким образом можно прийти к данной форме уравнения. [8]
Найти кажущийся порядок реакции, исходя из предположения, что скорость реакции определяется скоростью диффузии через уже прореагировавший слой; объяснить, каким образом можно прийти к данной форме уравнения. [9]
Величина кажущегося порядка реакции зависит от интервала концентраций, в котором производятся измерения. В работах [19] и [20] наблюдались иные, чем в работе [15], порядки реакции полимеризации, когда растворителями служили циклогексан, 1 2-дихлорэтан и нитробензол. Это расхождение можно объяснить тем, что в работе [19] не было учтено влияние примесей воды, а в работе [20] не принимали во внимание влияние примесей формальдегида. [10]
Экспериментально определить кажущийся порядок реакции можно по характеру зависимости скорости процесса от температуры. Проведенные нами опыты по взаимодействию графита с двуокисью углерода в интервале температур 673 - 973 К показали прямолинейную зависимость скорости процесса от температуры, что подтверждает первый порядок реакции C COj в данном температурном интервале. [11]
Примечательно, что кажущийся порядок реакции остается первым по реагенту А, диффузия которого затруднена, тогда как порядок реакции по реагенту В уменьшается вдвое. [12]
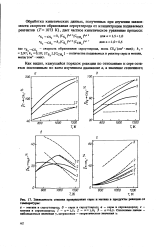 |
Зависимость степени превращения серы в метана в продукты реакции от температуры. [13] |
Как видно, кажущийся порядок реакции по отношению к сере остается постоянным во всем изученном диапазоне о, а значение степенного. [14]
 |
Влияние на выход продуктов размеров частиц графитовой насадки. [15] |
Страницы: 1 2 3 4