Бьер-рум
Cтраница 2
Итак, имеется очень хорошая функция п и ее зависимость от равновесной концентрации лиганда. Решение системы уравнений для w f ( [ L ]) принципиально не имеет препятствий, но составляет значительный труд. Сейчас уже этим занимаются ЭВМ, но наиболее простое решение предложено тем же Бьер-румом и с успехом применяется химиками. [16]
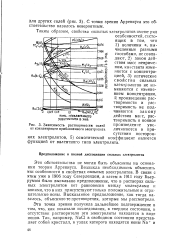 |
Зависимость растворимости солей от концентрации прибавленного электролита. [17] |
Эти обстоятельства не могли быть объяснены на основании теории Аррениуса. Возникла необходимость объяснить эти особенности в свойствах сильных электролитов. В связи с этим уже в 1906 году Сезерлендом, а затем в 1911 году Бьер-румом было высказано предположение, что в растворах сильных электролитов нет равновесия между молекулами и ионами, что в них присутствуют только положительные и отрицательные ионы. [18]
Справедливо также следующее общее правило: введение нуклео-фильных заместителей повышает, а введение электрофильных - снижает устойчивость хелатов металлов. Этот эффект должен проявляться особенно четко, если заместители связаны непосредственно с донорным атомом. Это возможно прежде всего для донорного атома азота. Бьер-рум [232, 1345] сравнил константы устойчивости комплексов серебра с монодентатными аминами в качестве лигандов ( для которых справедливы те же закономерности, причем они более ярко выражены) с величинами рКа аминов и нашел, что в этом случае также существует линейная зависимость. Даже гетероциклические амины располагаются в одном ряду с алифатическими. Для хелатов с соответствующими аминными лигандами в общем сохраняется та же последовательность, однако при образовании хелатов большее значение приобретают стерические эффекты. [19]
При этом следует пользоваться константами ионизации, экстраполированными к нулевому значению ионной силы, так как присутствие солей изменяет электростатические взаимодействия, в результате чего коэффициенты активности становятся отличными от единицы. Разности Ар / Са - log 4, приведенные в третьем столбце табл. 7, определяют вклад электростатических взаимодействий в изменение константы второй ступени ионизации. В столбцах 4 и 5 приведены расстояния г между центром отрицательного заряда молекулы и отщепляемым протоном, найденные соответственно из предположения о максимально вытянутой конфигурации молекулы и из предположения о свободном вращении вокруг всех связей. В столбце 6 приведены значения г, вычисленные на основании теории Бьер-рума. Для глутаровой кислоты и кислот с еще большим молекулярным весом эти значения, промежуточные между значениями г в столбцах 4 и 5, вполне правдоподобны; однако для низших кислот величина г оказывается, так же как и для глицина, слишком малой. [20]
 |
Ход нервных волокон в сетчатке. Черные участки указывают на те волокна, поражение которых характерно для глаукомы ( по Harrington. [21] |
Исключением является парамакулярная зона, расположенная примерно в 10 - 20 от центральной ямки. Нервные волокна в этой зоне представляют собой пучок, имеющий дугообразный ход от горизонтального шва в носовой половине до ДЗН. По форме этот пучок напоминает веер, широкая часть которого находится у горизонтального шва, а узкая у диска зрительного нерва. Непосредственно в ДЗН дугообразный пучок нервных-волокон находится в крайне стесненных условиях, будучи отодвинутым к верхнему и нижнему полюсам ДЗН папилло-макулярным пучком. Участок поля зрения, соответствующий этому пучку нервных волокон, получил название зоны Бьер-рума. Одновременное поражение верхнего1 и нижнего пучков приводит к образованию кольцевой скотомы. [22]
Страницы: 1 2