Последовательность - аминокислота
Cтраница 1
Последовательность аминокислот, ковалентно связанных между собой в полипептиде, представляет собой первичную структуру белка. [1]
Последовательность аминокислот в молекуле инсулина человека показана на рис. 14.4. Следует обратить внимание, что символ Су-S использован для обозначения половины молекулы цистина. [2]
Последовательность аминокислот в коротких линейных пептидах ( и особенно в циклопептидах) успешно определяют с помощью масс-спектрометрии. [3]
 |
Последовательность аминокислот в молекуле бычьего инсулина. [4] |
Последовательность аминокислот в пептидных цепях белков, например инсулина, производит впечатление случайной и лишенного систематичности набора; однако она может оказывать влияние на свойства белков несколькими способами. Так, кислотно-основные свойства белков и их изоэлектриче-ские точки определяются числом и расположением кислых в основных аминокислот. Пространственное влияние замещающих групп определяет стабильность и точки изгиба пептидных спиралей. Последовательность аминокислот также может оказывать влияние на степень межмолекулярных взаимодействий и растворимость белков. Пептиды, состоящие из аминокислот одного типа, часто оказываются чрезвычайно малорастворимыми вследствие сильных внутримолекулярных взаимодействий. Если однородность цепи нарушается в результате включения в нее других аминокислот, то можно ожидать, что внутримолекулярные взаимодействия будут ослаблены. [5]
Последовательность аминокислот в любом белке определяется последовательностью оснований в определенных участках ДНК той клетки, в которой данный белок продуцируется. Эта информация передается от ДНК на белоксинтезирующий механизм в рибосомах с помощью информационной РНК. Однако в белках, как известно, обычно присутствует двадцать различных аминокислот, тогда как в нуклеиновых кислотах имеется только четыре основных типа нуклеотидов. [6]
Последовательность аминокислот в каждом белке ( первичная структура) задается генетически; укладка этой цепочки в глобуле ( наз. Третичную структуру стабилизируют водородные связи, нан-дер-наальсовы силы, гидрофобные взаимодействия, а также солевые и дисульфидные мостики. [7]
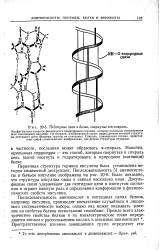 |
Пептидные цепи в белке, свернутые в а-спираль. [8] |
Последовательность аминокислот в пептидных цепях белков, например инсулина, производит впечатление случайного и лишенного систематичности набора; однако она может оказывать влияние на свойства белков несколькими способами. [9]
Последовательность аминокислот может также оказывать влияние на степень межмолекулярных взаимодействий и растворимость белков. Пептиды, состоящие из аминокислот одного типа, часто оказываются чрезвычайно мало растворимыми вследствие сильных внутримолекулярных взаимодействий. Если однородность цепи нарушается в результате включения в нее других аминокислот, то можно ожидать, что внутримолекулярные взаимодействия будут ослаблены. [10]
Последовательность аминокислот в химотрипсине устанавливается в настоящее время с помощью методов, описанных выше для инсулина; способ, которым закручены и согнуты цепи, будет по-видимому, установлен методом рентгеноструктурного анализа, как это было сделано для миоглобина. [11]
Последовательность аминокислот в пептидных цепях белков, например инсулина, производит впечатление случайного и лишенного систематичности набора; однако она может оказывать влияние на свойства белков несколькими способами. Так, кислотно-основные свойства белков и их изоэлектрические точки определяются числом и расположением кислых и основных аминокислот. Пространственное влияние замещающих групп определяет стабильность и точки изгиба пептидных спиралей. Последовательность аминокислот также может оказывать влияние на степень межмолекулярных взаимодействий и растворимость белков. Пептиды, состоящие из аминокислот одного типа, часто оказываются чрезвычайно мало растворимыми вследствие сильных внутримолекулярных взаимодействий. [12]
Последовательность аминокислот установлена Сейнджером ( 1949 - 1954), см. схему на стр. [13]
Последовательность аминокислот в пептидных цепях белков, например инсулина, производит впечатление случайного и лишенного систематичности набора; однако она может оказывать влияние на свойства белков несколькими способами. Прежде всего электрические свойства белков и их изоэлектрические точки определяются числом и расположением кислых и основных аминокислот. Пространственное влияние замещающих групп определяет стабильность и точки изгиба пептидных спиралей. Последовательность аминокислот также может оказывать влияние на степень межмолекулярных взаимодействий и растворимость белков. Пептиды, состоящие из аминокислот одного типа, часто оказываются чрезвычайно мало растворимыми вследствие сильных внутримолекулярных взаимодействий. Если однородность цепи нарушается в результате включения в нее других аминокислот, то можно ожидать, что внутримолекулярные взаимодействия будут ослаблены. [14]
Последовательность аминокислот установлена Сепнджером ( 1949 - 1951), см. схему на стр. [15]
Страницы: 1 2 3 4