Последовательность - реакционная способность
Cтраница 1
Последовательность реакционной способности - третичный вторичный первичный - является той, которой и следовало ожидать, так как известно, что электронодефицитные центры стабилизируются алкильными группами в большей степени, чем водородом, вследствие меньшей способности алкильиых групп к оттягиванию электронов ( см. стр. [1]
Последовательность реакционной способности - третичный вторичный первичный - является той, которой и следовало ожидать, так как известно, что электронодефицитные центры стабилизируются алкильными группами в большей степени, чем водородом, вследствие меньшей способности алкильных групп к оттягиванию электронов ( см. стр. [2]
Далее, последовательность реакционной способности галогенов изменяется в противоположном направлении по сравнению с предыдущим случаем. [3]
 |
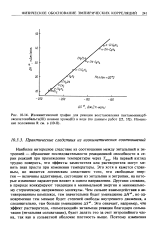
Температурная зависимость обмена бутена-1 с дейтерием на Pd / Al2O3 ( анализы при степени превращения 20 %. [4] |
Это соотношение не является последовательностью реакционной способности в процессе изомеризации. [5]
Как и следовало ожидать, последовательность реакционных способностей хорошо согласуется с рядом стабильности радикалов, ожидаемой на основании резонансной стабилизации. [6]
Как и следовало ожидать, последовательность реакционных способностей хорошо согласуется с рядом стабильности радикалов, ожидаемой на основании резонансной стабилизации. Вынужденная копланарность радикала является, по-видимому, важным фактором для достижения максимума резонансной стабилизации; об этом свидетельствует тот факт, что флуоренильный радикал оказывается более устойчивым, чем дифенил метил - радикал. [7]
 |
Изокинетический график для реакции восстановления пентамминкарб-оксилатокобальта ( Ш ионами хрома ( П в воде ( по данным работ. Изменение положения R в ( 10 - П. [8] |
Наиболее интересное следствие из соотношения между энтальпией и энтропией - обращение последовательности реакционной способности в серии реакций при прохождении температуры через Гизо. На первый взгляд трудно поверить, что эффекты заместителя или растворителя могут менять знак просто при изменении температуры. Это хотя и кажется странным, но является логическим следствием того, что свободные энергии величины аддитивные, состоящие из энтальпии и энтропии, на которые изменение параметров влияет в одном направлении. Другими словами, в природе конкурируют тенденции к минимальной энергии и минимальному стерическому напряжению молекулы. [9]
В отсутствие свободного основания, то есть при использовании только пиперидида лития в эфире, последовательность реакционной способности фенилгалогени-дов изменяется на обратную, оставаясь качественно той же для амидов и литийорганических реагентов: фтор-бензол - быстрее, чем бромбензол, и далее с небольшими интервалами - хлор - и иодбензол. [10]
В процессе превращения субстрата в молекулу 6 лимитирующей стадией может быть либо отрыв протона, либо последующая потеря галогенид-иона. Необычная последовательность реакционной способности уходящих групп ( Вг1С1) объясняется тем, что меняется стадия, определяющая скорость. Когда уходящей группой является Вг или I, лимитирующей стадией будет отрыв протона, и порядок скорости для этой стадии соответствует последовательности: FClBrI. Когда же уходящей группой является С1 или F, лимитирующим становится расщепление связи С-X, и порядок скорости для этой стадии соответствует последовательности: IBrClF. Подтверждение последнему факту было найдено при изучении конкурентных реакций. В таких соединениях наиболее кислый водород расположен между двумя атомами галогенов; когда он отрывается, остающийся анион может терять любой атом галогена. [11]
На самом же деле фторбензол участвует в реакции [ а ], поскольку в этой системе наблюдается быстрый дейтерообмен с образованием 2 - дейтерофторбензола33, однако поскольку в этом случае k2 существенно меньше, чем ft i ( BH), то образования Дегидробензола не происходит. Таким образом, последовательность реакционной способности, наблюдаемая в жидком аммиаке, характеризует перенос скорость лимитирующей стадии реакции от k2, для которой скорость падает в ряду I Вг С1 F, на fti, когда F C1 Вг I. Так как величина [ ВН ] входит в знаменатель выражения, определяющего скорость реакции, то добавление свободного амина должно уменьшать общую скорость, если величина k2 мала. Это положение справедливо для арилфтори-дов. [12]
 |
Относительная реакционная способность нуклеофилов по отношению к карбениевым ионам и бромистому метилу в водной среде. [13] |
Величины N представляют собой непосредственно наблюдаемые скорости реакции n - нитромалахитового зеленого ( 24) с нуклеофилами, logKOTH относится к конкурентной реакции трифенилметил-катиона, п - ну-клеофильная реакционная способность в реакциях согласованного замещения метилбромида. Сравнение приведенных величин обнаруживает существенное различие в последовательности реакционной способности ( например, по отношению к Ыз, ОН, S2O, ) между реакциями с участием карбениевых ионов и реакциями, проходящими по согласованному механизму. Причина такого несоответствия пока является предметом обсуждения. [14]
Наилучшие результаты достигаются при использовании арилбромидов и первичных алкилбромидов. Выход алкилбеизолов резко уменьшается для вторичных алкилбромидов и алкилйодидов, третичные алкилгалогеинды не вступают в эту реакцию. Такая последовательность реакционной способности становится понятной при рассмотрении механизма реакции. Первоначально из арилгалогеинда и натрия образуется арилнатрий. [15]
Страницы: 1 2