Последовательность - элементарная стадия
Cтраница 2
Последние годы отмечены интенсивным исследованием гомогенного катализа комплексами переходных металлов. Значительные успехи достигнуты в понимании ряда каталитических систем, включая спектроскопическую идентификацию или выделение реакцион-носпособных промежуточных продуктов, установление последовательности элементарных стадий и определение в некоторых случаях констант скорости и равновесия для этих стадий. Большое значение имел синтез сравнительно устойчивых каталитически неактивных модельных соединений, особенно переходных металлов третьего ряда, содержащих фрагменты, сходные с теми, которые постулируются для более реакционноспособных каталитически активных промежуточных соединений. [16]
В то же время исследования ЭНИН показали, что факел распыленного топлива в турбулентном потоке не является однородным; происходит горение как отдельных капель, так и их совокупностей. Однако, основываясь на ранее изложенных данных о горении индивидуальных капель, можно полагать, что горение тяжелого жидкого топлива будет развиваться в условиях более выраженного дискретного строения факела, при котором должна сохраниться вся последовательность элементарных стадий, хотя на длительность каждой из них будет оказываться влияние других капель, движущихся в непосредственной близости. [17]
Полная реакция может идти через несколько последовательных элементарных стадий. Если одна из них протекает медленнее других, то она является скорое гьопред ел иющей ( лимитирующей) стадией. Последовательность элементарных стадий, через которые протекает полная реакция, называется механизмом реакции. [18]
Каждая из перечисленных реакций может протекать по конкретному механизму. Описание химической реакции по стадиям называется механизмом. Следовательно, механизм реакции - это последовательность элементарных стадий, через которые осуществляется данная реакция. Различают свободно-радикальные, электрофильные и нуклео-фильные реакции. [19]
Каждая из перечисленных реакций может протекать по конкретному механизму. Описание химической реакции по стадиям называется механизмом. Следовательно, механизм реакции - это последовательность элементарных стадий, через которые осуществляется данная реакция. Различают свободно-радикальные, электрофильные и нук-леофильные реакции. [20]
Если порядок реакции по компоненту равен нулю, он не участвует в реакции и концентрацию в кинетическое уравнение не вносят. Порядки реакции определяют только экспериментально и на их основе расшифровывают механизм реакции. С другой стороны, возможен обратный прием установления механизма: вначале предполагают последовательность элементарных стадий ( включающих быстрые химические реакции и адсорбционные стадии) и записывают кинетические уравнения. [21]
Применение вычислительных машин дает возможность более полно использовать данные химической библиотеки. Программа, написанная на языке FORTRAN IV для вычислительной машины IBM 360 / 65, позволяет установить последовательность элементарных стадий, в которых один ион или группа ионов может быть отделена от других мешающих ионов. Программа состоит из ряда логических операций над матрицей химической информации, в которой поведение различных ионов относительно всех пар сорбент - среда ( кратко пара С / 5) закодировано специальным способом. [22]
Можно отметить, что как раз в данном случае существует наиболее подходящая ситуация для замены радиальной скорости роста удельной скоростью реакции на границе раздела. Поскольку при этом скорость зародышеобразования практически ни на что не влияет, имеется реальная возможность найти общую зависимость скорости реакции от температуры и давления, если, конечно, известны последовательность элементарных стадий для данной реакции и лимитирующая стадия. [23]
Однако первой моделью в системе частных моделей любого реактора является кинетическая модель. Кинетическая модель - совокупность стадий реакций и уравнений, характеризующих зависимость скорости реакции по стехиометрическому базису маршрутов реакции от концентраций реагирующих веществ, температуры и давлений во всей области их изменений, охватывающей практические условия реализации процессов. Кинетическая модель также строится по иерархическому принципу. Кинетика сложной реакции определяется последовательностью элементарных стадий и свойствами катализатора. Кинетическая модель, составленная на основе глубокого анализа механизма реакции, позволяет делать более надежные выводы и рекомендации по сравнению с эмпирическим описанием. Эмпирические кинетические уравнения могут сильно различаться при примерно равной точности описания экспериментальных данных. Лля определения температурного и концентрационного полей ъ слое катализатора и других задач, при которых не требуется знание производных скорости реакции по маршруту, результата, полученные на основе эмпирических и теоретических моделей практически равноценны. Однако, при определении оптмальных условий и решения других задач моделирования часто тебуется знание производных от скорости реакции. Оптимальнее режимы могут сильно отличаться в зависимости от вида кинетической модели, хотя исходные уравнения, могут приблизительно одинаково описывать экспериментальные давние о скорости химических превращений. [24]
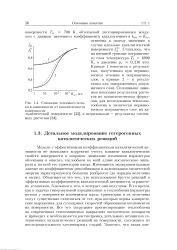 |
Снижение теплового потока в зависимости от каталитичности. [25] |
Модели с эффективными коэффициентами каталитической активности не позволяют корректно учесть влияние каталитических свойств поверхности в широком диапазоне изменения параметров обтекания и описать теплообмен по всей длине космического аппарата и на всей его траектории входа. Объясняется это тем, что использование брутто реакций и эффективных коэффициентов каталитической активности, ограничено условиями, близкими к тем, в которых они получены. В то время, в задачах гиперзвуковой аэродинамики и теплообмена параметры потока у поверхности изменяются вдоль траектории и их величины могут существенно отличаться от тех, при которых верны эмпирические выражения для суммарных скоростей образования компонентов на поверхности. Все это затрудняет прогнозирование теплообмена на современных теплозащитных покрытиях космических аппаратов и приводит к необходимости рассмотрения детального механизма гетерогенных каталитических реакций на поверхности, состоящего из последовательности элементарных стадий. [26]
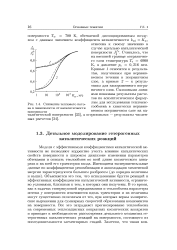 |
Снижение теплового потока в зависимости от каталитичности. [27] |
Модели с эффективными коэффициентами каталитической активности не позволяют корректно учесть влияние каталитических свойств поверхности в широком диапазоне изменения параметров обтекания и описать теплообмен по всей длине космического аппарата и на всей его траектории входа. Объясняется это тем, что использование брутто реакций и эффективных коэффициентов каталитической активности, ограничено условиями, близкими к тем, в которых они получены. В то время, как в задачах гиперзвуковой аэродинамики и теплообмена параметры потока у поверхности изменяются вдоль траектории и их величины могут существенно отличаться от тех, при которых верны эмпирические выражения для суммарных скоростей образования компонентов на поверхности. Все это затрудняет прогнозирование теплообмена на современных теплозащитных покрытиях космических аппаратов и приводит к необходимости рассмотрения детального механизма гетерогенных каталитических реакций на поверхности, состоящего из последовательности элементарных стадий. [28]
В этой главе мы обсудим кинетические закономерности реакции водорода с кислородом при высоких температурах и проследим их взаимосвязь с механизмом реакции при низких температурах. Именно с помощью метода ударной трубы удалось не только детально исследовать кинетический механизм быстрой реакции водорода с кислородом, но и количественно определить константы скоростей наиболее важных элементарных стадий. Сначала рассмотрим некоторые главные кинетические особенности быстрых цепных процессов при высоких температурах. Сравним метод ударной трубы с другими экспериментальными методами, обеспечивающими химиков важной количественной информацией о реакции водорода с кислородом. Рассмотрим различные методики регистрации в ударной трубе и информацию, получаемую с их помощью. Но основное внимание уделим последовательности элементарных стадий в полном механизме реакции водорода с кислородом и константам скоростей этих элементарных стадий. [29]
При комнатной температуре NO2 и NO газообразны. Если их концентрации превышают растворимости, они улетучиваются, не успев прореагировать. Так происходит при высокой кислотности, когда скорость реакции велика и промежуточные соединения накапливаются в больших количествах. Этим можно объяснить выделение NO2 из концентрированных растворов HNO3, тогда как в более разбавленных растворах NO2 успевает восстановиться до NO, прежде чем ее концентрация превысит растворимость. Однако NO растворима гораздо хуже, чем NO2, и поэтому может выделяться из раствора. Этот переход через промежуточные состояния окисления ( HNO3 - - N02 - vNO - NHt) не представляет собой последовательности элементарных стадий, так как каждый переход является сложной реакцией. Однако существуют некоторые указания на то, что восстановление HN03 действительно идет через эти промежуточные вещества. [30]
Страницы: 1 2 3