Последовательность - уровни
Cтраница 1
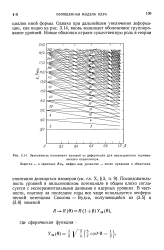 |
Зависимость положения уровней от деформации для неизотропного гармонического осциллятора. Энергия - в единицах Й ( 00. цифры над уровнями - число нуклонов в оболочках. [1] |
Последовательность уровней в нильсеновском потенциале в общем плохо согласуется с экспериментальными данными о ядерных уровнях. [2]
 |
Энергетические уровни молекулярных орбиталей, показанных на 12 - 7. Среди молекулярных орбиталей, образованных атомными s - и р-орбиталями, связывающие устойчивее. [3] |
Такая последовательность уровней установлена тщательными современными исследованиями спектроскопических и магнитных свойств молекулярных частиц В2 и NJ. Эта последовательность поддается объяснению, потому что электроны, поступающие на молекулярную орбиталь пх, больше отдалены в пространстве от электронов на CTS - и of - орбиталях, чем если бы они поступали в первую очередь на оуорбиталь. При переходе к более тяжелым элементам второго периода, начиная с кислорода, происходит обращение энергетических уровней, поэтому у О2 и F2 орбиталь az более устойчива, чем лх и ку. Однако для нашего обсуждения это не имеет значения, поскольку в О2 и F2 все три обсуждаемых уровня уже заполнены электронами. Орбитали ях и пу имеют одинаковую энергию или, как говорят, соответствуют вырожденному энер - 1егическому уровню. [4]
Для установления последовательности уровней экспериментально нужно выяснить, является ли рассматриваемый элемент НМО первичным структурным образованием, или, в свою очередь, собран из более простых элементов. [5]
С открытием кварков последовательность уровней строения материи приобрела вид: кварки, адроны, атомные ядра, атомы. Это поразительным образом совпадает с предвидением Ньютона, который три века назад, в 1704 г., написал: Мельчайшие частицы материи могут сцепляться посредством сильнейших притяжений, составляя большие частицы, но более слабые; многие из них могут также сцепляться и составлять еще большие частицы с еще более слабой силой - и так в ряде последовательностей, пока прогрессия не закончится самыми большими частицами, от которых зависят химические действия и цвета природных тел; при сцеплении таких частиц составляются тела заметной величины... Таким образом, в природе существуют агенты, способные сжимать вместе частицы тел весьма сильными притяжениями. [6]
Такой качественный вывод последовательности уровней, вообще говоря, оказывается невозможным для гетероядерных двухатомных молекул. Атомные орбитали одинакового типа, но принадлежащие двум химически различным атомам, имеют неодинаковые энергии. Их основные взаимодействия могут осуществляться с орбиталями иного типа на другом атоме, а не с орбиталями того же типа. Даже качественное обсуждение молекулярно-орбитальных энергетических уровней для таких молекул обычно требует обращения к методам, описанным в гл. В очень редких случаях атомы молекулы обладают достаточно сходными свойствами, чтобы их молекулярно-орби-тальные энергетические уровни удалось аппроксимировать изображенными на рис. 11.2. Наиболее примечательным примером таких молекул является СО. Несмотря на то что атомные орбитали кислорода по энергии расположены ниже, чем у углерода, возникающие молекулярные орбитали имеют энергетические уровни, расположение которых напоминает схему уровней гомоядерных двухатомных молекул. В частности, энергия диссоциации СО лишь слегка превышает таковую для N2 ( 257 ккал / моль), и молекула имеет очень малый ди-польный момент. [7]
Согласно правилу Гунда, последовательность уровней обращается ( уровни с меньшими / оказываются выше, чем уровни с большими /) при изменении знака постоянной спин-орбитального взаимодействия. Это можно объяснить, рассматривая вместо системы, в которой по орбиталям движутся электроны, систему, в заполненой оболочке которой движутся дырки. Дырка несет заряд, противоположный заряду электрона, что и объясняет инверсию / - уровней, а также отклонение g - фактора в сторону значений, больших чем для свободного спина. [8]
 |
Расщепление d - уровней в кристаллических полях различной симметрии. [9] |
На основании качественных соображений невозможно однозначно определить последовательность уровней. DM) должна быть наименее устойчивой, поскольку она направлена своими пучностями к лигандам, а орбиталь d ( alg в группе D4u) наиболее устойчивой, поскольку ее пучности направлены перпендикулярно плоскости ху. [10]
Заметим, что при L - - x последовательность уровней становится строго непрерывной, так как А. [11]
Для размещения переходов в схеме уровней и установления последовательности уровней и их энергии полезен комбинационный принцип Ритца, из к-рого следует, в частности, что если сумма энергий двух Y-ЛИНИЙ равна энергии третьей линии, то первые 2 перехода идут в каскаде друг за другом параллельно 3-му - прямому переходу. Этот метод обобщается на каскады из большого числа а -, Р - и у-пе Рех Д в - Для размещения переходов и уровней в схеме измеряются YY - PY и ДР - совпадения. Если 2 частицы регистрируются практически одновременно, то оба перехода следуют в каскаде друг за другом. [12]
 |
Схематическое расположение электронно-колебательных уровней энергии многоатомной молекулы. [13] |
На основании такого подхода можно заключить, что вся последовательность уровней выбранной системы может быть представлена следующим образом: около каждого уровня энергии легкой частицы будет располагаться группа уровней энергии тяжелой частицы. [14]
Третье правило основано на учете магнитных взаимодействий, так как последовательность уровней определяется спин-орбитальным взаимодействием. Обращение уровней в том случае, когда оболочка заполнена более чем наполовину, отражает изменение знака постоянной спин-орбитальной связи. [15]
Страницы: 1 2 3 4