Замедление - распад
Cтраница 2
Имеющиеся в литературе сведения о влиянии давления на скорость термического крекинга индивидуальных парафиновых углеводородов ( при постоянной температуре) относятся к области небольших давлений. В работе Динцеса [1] приведены данные, показывающие, что скорость термического распада н-бутана при 575 С увеличивается при повышении давления с 3 9 до 10 8 атм. Динцес, Жаркова, Жерко и Фрост [2] обнаружили замедление распада этана при повышении давления с 1 до 26 атм и температуре 635 С. Исследование термического распада - гептана при 580 С и давлении до 8 7 атм [4] также обнаружило увеличение скорости реакции с повышением давления. [16]
Причиной замедления распада переохлажденного легированного аустенита в области диффузионного превращения является то, что в процессе образования перлита принимают участие легирующие элементы. Образованию ферри го-карбидной смеси предшествует диффузия в аустените не только углерода, но и легирующих элементов - карбидообразующие элементы концентрируются в основном в карбидной фазе с образованием легированного цементита или специальных карбидов, а некарбидообразующие элементы - в феррите. Скорость диффузии легирующих элементов во много раз меньше скорости диффузии углерода, поэтому замедление аустенито-перлитного распада определяется малой скоростью диффузии легирующих элементов. [17]
Механизм распада гидроперекиси в присутствии StaCu, по-видимому, заключается в следующем. Стеарат меди обравует с гидроперекисью комплекс, который распадается далее с образованием свободного радикала и одновалентной меди. Последняя медленно реагирует с гидроперекисью; поэтому изменение валентного состояния меди приводит к замедлению распада гидроперекиси. [18]
Механизм распада гидроперекиси в присутствии St2Gu, по-видимому, заключается в следующем. Стеарат меди образует с гидроперекисью комплекс, который распадается далее с образованием свободного радикала и одновалентной меди. Последняя медленно реагирует с гидроперекисью; поэтому изменение валентного состояния меди приводит к замедлению распада гидроперекиси. [19]
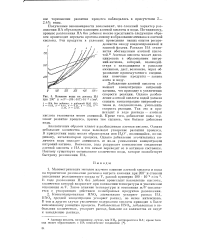 |
Влияние воды на распад НА при 200 и m / F ( 89 - 107 - 10 - 4 г / см3. [20] |
Концентрированная HNOa значительно ускоряет распад НА, IIN03 средней концентрации ускоряет распад, но менее интенсивно. В том и другом случае увеличение содержания кислоты приводит к более интенсивному развитию процесса. Разбавленная HNOS, добавленная в небольших количествах, ускоряет распад, большие же количества ее ведут к замедлению распада. [21]
Нейтрализация эмульгатора кислотой1 4 необходима для перевода ПАВ в форму соли. Степень нейтрализации, которую можно выразить количеством ( в кг) добавляемой кислоты на 1 кг эмульгатора, составляет обычно 0.2 - 0.5 и оказывает большое влияние на свойства конечной эмульсии. Повышение кислотности водной фазы ( соответственно - понижение водородного показателя рН) способствует повышению стабильности эмульсии при хранении и замедлению распада на поверхности, но улучшать эти показатели за счет большого избытка кислоты не рекомендуется, т.к. это может привести к снижению адгезии. [22]
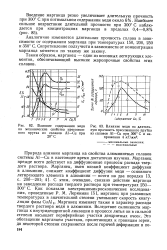 |
Влияние меди на длительную прочность прессованного прутка из сплавов А1 - Си при 300 С и напряжении 4 кГ / мм2. [23] |
Природа влияния марганца на свойства алюминиевых сплавов системы А1 - Си в настоящее время достаточно изучена. Марганец прежде всего действует на диффузионные процессы распада твердого раствора. Марганец, имея низкий коэффициент диффузии в алюминии, снижает коэффициент диффузии меди - основного легирующего элемента в алюминии - почти на два порядка [ 3, с. С этим, очевидно, связано действие марганца на замедление распада твердого раствора при температурах 250 - 300 С. Марганец изменяет также и характер распада твердого раствора меди в алюминии. Вследствие склонности марганца к внутридендритнои ликвации в процессе литья он в сильной степени насыщает периферийные участки дендритных ячеек. [24]
ПВХ в разбавленных растворах линейно повышается с увеличением содержания диметиламина. При экстраполяции этой зависимости на нулевую концентрацию диметиламина была определена скорость дегидрохлорирования ПВХ в абсолютно чистом диметилформамиде. Она оказалась равной 7 8 - Ю 7 моль НС1 / ( гПВХ - мин), что на 2 десятичных порядка выше, чем для блочного ПВХ при той же температуре, но на 2 - 3 порядка меньше, чем в присутствии диметиламина. Таким образом, наличие примеси диметиламина является основной причиной высокой начальной скорости дегидрохлорирования ПВХ. Казалось бы, что дегидрохлорирование, приводящее к связыванию свободного диметиламина и повышению кислотности среды, должно способствовать замедлению распада ПВХ. [25]
Различают экстенсивную и интенсивную регуляцию активности ферментов в клетках и тканях организма. Экстенсивная регуляция обусловлена индукцией или репрессией генов, кодирующих синтез соответствующих ферментов. Увеличение или уменьшение числа активных молекул определяет суммарную активность пула данного фермента в каком-либо компартменте клетки, в ткани или целом органе. В физиологических условиях содержание того или иного фермента в клетке постоянно и регулируется двумя процессами: скоростью его синтеза и распада. Оба эти процесса взаимосвязаны и контролируются на генном уровне. Увеличение скорости синтеза ферментативного белка обусловливает активацию внутриклеточных протеиназ и ускоренный распад старых молекул фермента, а снижение скорости синтеза приводит к замедлению распада ферментативного белка. [26]
Страницы: 1 2