Потенциал - ионизация
Cтраница 4
Потенциал ионизации, связанный с л-орбиталью, быстро убывает вследствие усиления эффекта индукции ( И) со стороны замещающих алкильных групп. [46]
Потенциал ионизации - энергия, которую необходимо затратить для отрыва наиболее слабо связанного электрона от атома. [47]
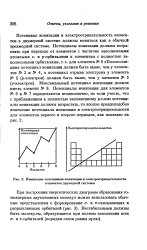 |
Изменение потенциала ионизации и электроотрицательности элементов двумерной системы. [48] |
Потенциал ионизации и электроотрицательность элементов в двумерной системе должны меняться как в обычной трехмерной системе. Плосколан-дии потенциал ионизации должен быть выше, чем у элементов № 3 и № 4, а потенциал отрыва электрона у элемента JV. [49]
Потенциалы ионизации уменьшаются от серы к теллуру, что свидетельствует об усилении в этом направлении металлических свойств. [50]
Потенциал ионизации ( /), выраженный в - вольтах ( В), численно равен энергии ионизации ( Е), выраженной в электронвольтах. [51]
Потенциал ионизации ( сокращенно ПИ) атома представляет собой минимальную энергию, необходимую для полного удаления электрона из атома. [52]
Потенциалы ионизации, определяемые по разным методикам, могут отличаться даже на несколько электронвольт. Однако, ввиду несомненной грубости допущенных при формулировке метода МВГ приближений, вряд ли точность расчета потенциалов ионизации имеет существенное значение. Главным методологическим требованием здесь является, по-видимому, требование использовать в расчетах рядов соединений потенциалы ионизации, полученные для всех встречающихся в расчетах элементов по одной и той же методике. [53]
Потенциалы ионизации всех редкоземельных элементов равны примерно 6 эв. [54]
Потенциал ионизации и энергетическая щель между занятыми и свободными состояниями уменьшаются, а сродство к электрону и энергия связи, приходящаяся на один атом, увеличиваются с ростом кластера. Для металлов с нечетным числом электронов на фоне этих зависимостей наблюдаются осцилляции, обусловленные некоторым различием в свойствах кластеров с четным и нечетным числом атомов. [55]
 |
Потенциалы ионизации некоторых элементов. [56] |
Потенциалы ионизации этих элементов очень близки друг к другу, поэтому s - уровни А11 и р-уровни BV1 свободных атомов лежат примерно на одинаковой глубине. Зона проводимости должна возникать из s - уров-ней элемента А и должна быть тем самым простой. [57]
Потенциалы ионизации я вляются важной характеристикой атомов и могут быть непосредственно измерены. Величины потенциалов ионизации являются сложной функцией ряда свойств атомов: величины заряда ядра, атомного радиуса, экранирующего действия электронных подуровней, глубины проникновения внешних электронов в нижерасположенные электронные облака. [58]
Потенциал ионизации - это энергия, необходимая для удаления электрона из атома. Сродство к электрону - энергия, выделяющаяся в результате присоединения электрона. [59]
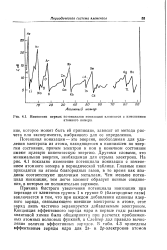 |
Изменение первых потенциалов ионизации элементов с изменением. [60] |
Страницы: 1 2 3 4 5