Потенциал - минимум
Cтраница 2
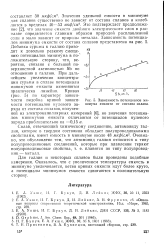 |
Зависимость потенциалов минимума емкости от состава сплава. [16] |
Это подтверждает предположение [2], что значение емкости двойного электрического слоя в расплаве определяется главным образом природой расплавленной солн и мало зависит от природы металла. Добавка сурьмы к галлию приводит к довольно резкому смещению потенциалов минимума в по - ложительную сторону, что, вероятно, связано с большой поверхностной активностью Sb по отношению к галлию. При дальнейшем увеличении концентрации сурьмы в сплаве потенциалы минимумов емкости изменяются практически линейно. [17]
При использовании этого метода нахождения в необходимо учитывать осложнения, возникающие при определении значений емкости по импедансным измерениям из-за наложения на результаты измерений влияния реакций растворения металла и восстановления деполяризатора, скорости которых зависят от степени заполнения. Этот метод применим лишь вблизи потенциала максимума электрокапиллярной кривой или потенциала минимума емкостной кривой при больших заполнениях. [18]
Такое совпадение обусловлено, как будет показано в главе V, наводораживанием катода в процессе электрохимической реакции. Так как емкость в точке минимума снижается по мере разбавления электролита, а величина потенциала минимума не зависит от частоты переменного тока, то можно считать потенциал - 0 6 нулевой точкой германия. [20]
В противном случае наклон называют отрицательным. При прочих равных условиях наклоны пиков тем больше, чем дальше располагаются потенциалы пиков от потенциала минимума тока на вольтамперограмме раствора без ЭАВ. Как правило, этот потенциал совпадает с потенциалом электрокапиллярного максимума. [22]
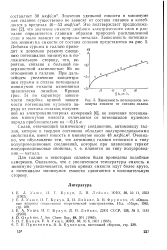 |
Зависимость потенциалов минимума емкости от состава сплава. [23] |
Для галлия и некоторых сплавов были проведены подобные измерения. Оказалось, что с увеличением температуры емкость в минимуме увеличивается, ветви кривых емкости идут более круто, а потенциалы минимумов емкости сдвигаются в положительную сторону. [24]
Кривая зависимости емкости от потенциала в большинстве случаев имеет форму симметричной параболы. Потенциал минимума С - ф кривой близок к потенциалу нулевого заряда, а величина емкости в минимуме является характеристической величиной, определяемой, в основном, составом и свойствами солевой фазы. В зависимости от состава электролита [3, 4] и температуры [5, 6] получены значения емкости при потенциалах минимума порядка 20 - 70 мкф / см2, при этом температурный коэффициент емкости положителен и емкость возрастает с уменьшением радиуса катиона соли и увеличением радиуса аниона. [25]
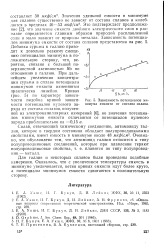 |
Зависимость потенциалов минимума емкости от состава сплава. [26] |
Это подтверждает предположение [2], что значение емкости двойного электрического слоя в расплаве определяется главным образом природой расплавленной солн и мало зависит от природы металла. Добавка сурьмы к галлию приводит к довольно резкому смещению потенциалов минимума в по - ложительную сторону, что, вероятно, связано с большой поверхностной активностью Sb по отношению к галлию. При дальнейшем увеличении концентрации сурьмы в сплаве потенциалы минимумов емкости изменяются практически линейно. [27]
Возражение это, однако, нам кажется неправильным. Частица PtfNH CU в целом действительно но может отталкиваться отрицательно заряженной поверхностью электрода, однако адсорбционная связь ее с поверхностью ртути, которая осуществляется при помощи несущих отрицательный заряд атомов хлора, должна ослабиться или разорваться при появлении на поверхности отрицательных зарядов. В общем можно утверждать, что частицы, подвергающиеся электровосстановлепию при потенциалах, более положительных с одной стороны и более отрицательных с другой, чем потенциал минимума поляризационной кривой, находятся в различных адсорбционных состояниях, которым соответствуют различные энергии активации. В первом случае мы имеем дело с притяжением положительно заряженной поверхностью аниона или входящих в состав частицы анионных групп, на которое в ряде случаев накладываются силы специфической адсорбции, благодаря чему адсорбция может происходить и при довольно значительных отрицательных зарядах поверхности. Что касается механизма протекания процесса при сильно отрицательных зарядах поверхности, то приближение к поверхности в этом случае, как было разъяснено в моем докладе, облегчается за счет образования катионных мостиков, что следует также рассматривать, как некоторую своеобразную форму адсорбции. Концентрация реагирующих частиц в поверхностном слое при этом, несомненно, мала и энергетические условия протекания процесса не выгодны; однако восстановление все же может происходить с достаточной скоростью благодаря снижению истинной энергии активации процесса, вызванному наличием большого отрицательного скачка потенциала на границе ртуть - электролит. В случае восстановления комплексов двухвалентной платины можно предположить, что связь с отрицательно заряженной поверхностью ртути осуществляется при помощи положительно заряженного центрального атома платины, если допустить, что эти частицы, обладающие нормально плоской конфигурацией, деформируются под влиянием электрического поли у поверхности электрода. [28]
 |
Осциллографи-ческая полярограмма.| Кривая анодного растворения. [29] |
Идея метода инверсионной полярографии состоит в выделении определяемого элемента из очень разбавленного раствора на ртутной капле или тонкой пленке ртути на графитовом электроде или просто на графитовом электроде электролизом с последующим анодным растворением полученной амальгамы. Процесс накопления происходит при потенциале, соответствующем предельному току. Зависимость силы тока от напряжения при анодном растворении имеет вид характерного пика ( рис. 10.9), глубина которого h пропорциональна концентрации определяемого иона, а потенциал минимума Ет п определяется природой иона. [30]
Страницы: 1 2 3