Потенциал - образование
Cтраница 1
Потенциалы образования непосредственно характеризуют устойчивость соединений только в отношении разложения на простые вещества. Что касается реакций других видов, то изменение изобарного потенциала для какойт либо химической реакции можно вычислить подобно тепловому эффекту путец алгебраического сложения и вычитания уравнений реакций образования соединений, участвующих в данной реакции. [1]
Потенциал образования можно определять для любых состояний веществ и при любых условиях их существования, В качестве стандартных применяются условия, указанные выше. Простые вещества берутся в стандартном состоянии в форме, наиболее устойчивой для данного элемента в этих условиях. Потенциал образования, относящийся к этим условиям и к температуре 25 0 С, будем обозначать АС0бР, 298 и относить к одному молю соединения. [2]
Потенциал образования можно определить, очевидно, для любых состояний веществ и при любых условиях их существования. Однако удобно в качестве стандартных принять условия, когда парциальные давления каждого газообразного компонента равны единице ( 1 атм) или, в общем случае, активности равны единице. Простые вещества берутся в стандартном состоянии в форме, наиболее устойчивой для данного элемента в этих условиях. Потенциал образования, относящийся к этим условиям, принято обозначать AG 06p298 и относить к одному молю соединения. Значения AG 06p29s для разных веществ даны в виде таблиц в литературе. [3]
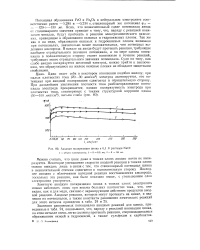 |
Анодная поляризация цинка в 0 1 N растворе NaCl. [4] |
Потенциал образования FeO и Fe203 в нейтральном электролите соответственно равен - 0 280 и - 0 234 в, стационарный же потенциал фст - 120ч - 130 мв. Ясно, что незначительный сдвиг потенциала анода от стационарного значения приведет к тому, что, наряду с реакцией ионизации металла, будут протекать и реакции электрохимического окисления, приводящие к образованию окисных и гидроокисных пленок. Так же как и на меди, образование окисных и гидроокисных пленок возможно при потенциалах, значительно менее положительных, чем потенциал выделения кислорода, В начале на аноде будут протекать реакции, требующие наиболее отрицательного значения потенциала, а по мере сдвига потенциала в положительную сторону станет возможным и течение реакций, требующих менее отрицательного значения потенциала. Судя по тому, как слабо анодно поляризуется железный электрод, можно прийти к заключению, что образующиеся на железе окисные пленки не обладают защитными свойствами. [5]
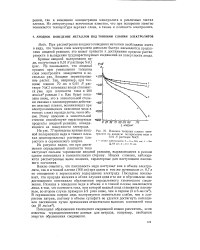 |
Влияние толщины пленки электролита на анодную поляризацию меди в 0 01 N растворе NaCl. [6] |
Потенциал образования химических соединений можно рассчитать, если известны термодинамические данные для металла, например, свободная энергия образования соединения. [7]
Стандартный потенциалы образования окислов на многих металлах отрицательнее потенциала кислородного электрода, поэтому в присутствии кислорода происходит окисление металла, это влияет на значение стационарного потенциала электрода. Существенное влияние на последний оказывает реакция восстановления кислорода до перекиси водорода. [8]
Оценить изобарно-изотермичеекий потенциал образования газообразного бутадиена-1 3 и газообразного ( условно) полибутадиена. [9]
Значения изобарно-изотермпческих потенциалов образования оксидов железа находят из справочников. [10]
По величинам стандартных изобарно-изотерми-ческих потенциалов образования газообразных диоксида и триоксида серы, соответственно равным - 71 7 и - 88 49 ккал / моль, следует допустить, что при окислении серы предпочтительнее образование триоксида. [11]
Используя значения стандартных изобарно-изо-термических потенциалов образования газообразных CF4, ССЦ, СВг4 и С14, соответственно равные - 212 3; - 14 5; 16 6 и 62 3 ккал / моль, сравнить устойчивость тетрагалоге-нидов углерода и оценить возможность их синтеза из простых веществ. [12]
Учитывая величины стандартного изобарно-изо-термического потенциала образования твердых гидридов бериллия, магния и кальция, соответственно равные 27 66; - 8 8 и - 32 6 ккал / моль, сделать вывод о возможности или невозможности прямого синтеза этих соединений из простых веществ. [13]
В настоящее время потенциалы образования известны для большого числа различных химических соединений и приводятся в соответствующих справочниках. [14]
Как видно, потенциалы образования окислов железа довольно близки и имеют отрицательные значения. [15]
Страницы: 1 2 3 4 5