Потенциал - образование
Cтраница 4
 |
Электрокапиллярная кривая ртути в 0 7 N раствор гидрата тетрабутиламмония с 0 1 TV концентрацией йодистого натрия. [46] |
Однако многочисленные дальнейшие исследования показали, что если проводить длительную поляризацию ртутного электрода при потенциалах образования второго максимума, последний уменьшается и через 30 - 40 мин электрокапиллярная кривая принимает обычную форму без второго максимума. В дальнейшем, при снятии электрокапиллярных кривых в достаточно концентрированном растворе хлористого тетрабутиламмония с добавкой йодистого натрия при длительной выдержке потенциалов были получены обычные кривые без вторых максимумов. [47]
После установления электрохимического равновесия между металлам и его ионами в растворе всегда должны преобладать те катионы, потенциал образования которых менее положителен. Равновесная концентрация катионов другой валентности уже при разности потенциалов порядка нескольких десятых вольта становится, как легко подсчитать, исчезающе малой. [48]
После установления электрохимического равновесия между металлом и его ионами в растворе всегда должны преобладать те катионы, потенциал образования которых менее положителен. Равновесная концентрация катионов другой валентности уже при разности потенциалов порядка нескольких десятых вольта становится, как легко подсчитать, исчезающе малой. [49]
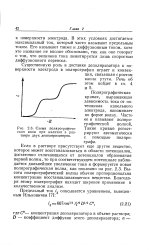 |
Схема полярографических волн при наличии в растворе двух деполяризаторов. [50] |
Если в растворе присутствует еще другое вещество, которое может восстанавливаться в области потенциалов, достаточно отличающихся от потенциалов образования первой волны, то при соответствующем потенциале наблюдается дальнейшее увеличение тока и формируется новая полярографическая волна, как показано на рис. 2.3. Высота полярографической волны обычно пропорциональна концентрации восстанавливающегося вещества. Благодаря этому полярография находит широкое применение в количественном анализе. [51]
При соответствующих значениях Кдиспр и констант скорости последующих реакций R и R2 восстановление может протекать через дианнон при потенциале образования анион-радика-ча. При исследовании в ДМФА гомологического ряда стильбенов, в котором имело место нарастание стерических факторов, затрудняющих образование плоской структуры, было установлено [129], что значения Кккспр тем больше, чем меиыце отличаются друг от друга потенциалы обеих стадий восстановления. [52]
 |
Потенциалы и плотности тока для образования безводного окисла железа. [53] |
Сравнение данных, приведенных в таблице, показывает, что в любом нк-гибирующем растворе потенциал неполяризованного образца всегда положитель-нее потенциала образования безводного окисла кубической структуры. [54]
 |
Кривая состав-напряжение для гидроксофторида ZrF ( OH3. [55] |
На основании данных настоящей работы построена кривая для гидроксофторидов циркония ( рис. 3), из которой следует, что потенциал образования фторида Zr3F2 ( OH) 10 равен - 100 В, a Zr5F ( OH) 19 - 400 В. [56]
Если сравнить значения стационарных потенциалов железа в нейтральных электролитах ( - 0 3 - - 0 5 в) со значениями потенциалов образования окисных слоев, то легко прийти к заключению, что уже при незначительном смещении потенциала от стационарного наряду с процессом ионизации происходит реакция электрохимического окисления. По мере смещения потенциала в положительную сторону процесс окисления все более усиливается, и при достижении потенциала пассивации электрод уже в значительной степени покрывается окисным слоем, приводящим к резкому уменьшению скорости ионизации металла; наступает явление пассивности. [57]
Сравнение значений стационарных потенциалов железа ( потенциалов коррозии) в нейтральных электролитах ( - 0 3 - - 0 4 В) со значениями потенциалов образования окислов железа приводит к выводу, что уже при незначительном смещении потенциала железа или стали в положительную сторону от стационарного параллельно процессу ионизации металла на электроде должна протекать реакция окисления, приводящая к возникновению на поверхности окисных слоев. [58]
Это тот же потенциал, что и наблюдаемый при появлении О; в чистом водяном паре; вместе с тем Робертсон делает вывод, что потенциал образования О из тригональной формы перекиси водорода не должен превышать 15 6 эв. Найденный потенциал 12 1 эв для образования Н2 ( Х ( очевидно, соответствует отрыву электрона кислородного атома перекиси водорода; этот электрон не участвует в образовании связи. [59]
При описании окислительно-восстановительных процессов уже отмечалось, что после установления электрохимического равновесия между металлом и раствором его катионов в растворе всегда должны преобладать те катионы, потенциал образования которых менее положителен. Равновесная концентрация катионов другой валентности уже при разности потенциалов ( ф / о-р 2 / о) порядка нескольких десятых вольта становится ис-чезающе малой. [60]
Страницы: 1 2 3 4 5