Потенциал - пробивание
Cтраница 1
Потенциал пробивания может быть использован в качестве количественной характеристики устойчивости пассивного состояния нержавеющих и кислотостойких сталей. [1]
Очень высокие значения потенциалов пробивания анодной окисной пленки на титане в нейтральных солевых растворах объясняют причины отсутствия склонности титана к питтинго-вой коррозии в водных средах электролитов. Столь высокие значения потенциалов пробивания, как в хлоро - и фтористосо-держащих растворах, не могут быть достигнуты в присутствии даже самых сильных окислителей. Потенциалы пробивания в йодо - и бромосодержащих растворах в принципе могут достигаться в растворах сильных окислителей, однако тогда в первую очередь будут разряжаться ионы брома и йода, имеющие менее положительные потенциалы, и достижение потенциалов пробивания будет затруднено. [2]
При достижении некоторого значения потенциала ( потенциала пробивания) защитная пленка на образце разрушается в одной или нескольких точках, вследствие чего значение электродного потенциала образца уменьшается. Наблюдается хорошее соответствие результатов сравнительных коррозионных испытаний хромистых и хромоникелевых сталей на точечную коррозию с данными, полученными методом определения потенциала пробивания. [4]
Склонность стали к точечной коррозии характеризуется значением потенциала пробивания V Пр, чем отрицательнее значение УПр, тем больше склонность стали к точечной коррозии. [5]
Как показала Н. К. Кернич, потенциал питтингообразова-ния Упо ( потенциал пробивания) находится в хорошем соответствии с очаговым показателем коррозии ( числом точек на 1 см2) и пригоден для исследования влияния различных факторов на точечную коррозию металлов. Существенное влияние на склонность к точечной коррозии оказывает природа металла. [6]
 |
Схема установки осциллографического определения сопротивления защитных пленок на. [7] |
Исследователь, как правило, интересуется не исходным значением потенциала пробивания, а его изменением во времени под воздействием окружающей среды. В ряде случаев, например, необходимо знать, изменяется ли контактная проводимость металлов, имеющих на поверхности окисные слои или гальванические покрытия. Для этой же цели удобно применять универсальную пробойную установку УПМ-1М, выпускаемую промышленностью. [8]
Электрические свойства защитных пленок, такие как электросопротивление, емкость, потенциал пробивания, представляют определенный интерес для исследователей коррозии, и их измерение находит все большее применение в практике для оценки защищенных свойств пленок. [9]
Возникновение точечной коррозии в данном случае объясняется достижением в результате анодной поляризации потенциала анодного пробивания пленки в отдельных почему-либо ослабленных участках поверхности сплава. [10]
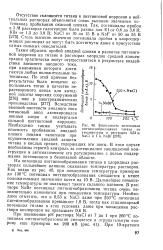 |
Зависимость потенциала питтингообразования титана от температуры в растворах 0 53 н. NaCl и 1 н. NaBr. [11] |
Отсутствие склонности титана к питтинговой коррозии в нейтральных растворах объясняется очень высоким значением потенциала пробивания окисной пленки. Столь высокие значения потенциала пробоя в хлорсодер-жащих растворах не могут быть достигнуты даже в присутствии самых сильных окислителей. [12]
Отсутствие склонности титана к питтинговой коррозии в нейтральных растворах объясняется очень высоким значением потенциала пробивания окисной пленки. [13]
Очень высокие значения потенциалов пробивания анодной окисной пленки на титане в нейтральных солевых растворах объясняют причины отсутствия склонности титана к питтинго-вой коррозии в водных средах электролитов. Столь высокие значения потенциалов пробивания, как в хлоро - и фтористосо-держащих растворах, не могут быть достигнуты в присутствии даже самых сильных окислителей. Потенциалы пробивания в йодо - и бромосодержащих растворах в принципе могут достигаться в растворах сильных окислителей, однако тогда в первую очередь будут разряжаться ионы брома и йода, имеющие менее положительные потенциалы, и достижение потенциалов пробивания будет затруднено. [14]
При достижении некоторого значения потенциала ( потенциала пробивания) защитная пленка на образце разрушается в одной или нескольких точках, вследствие чего значение электродного потенциала образца уменьшается. Наблюдается хорошее соответствие результатов сравнительных коррозионных испытаний хромистых и хромоникелевых сталей на точечную коррозию с данными, полученными методом определения потенциала пробивания. [15]
Страницы: 1 2
