Потенциал - свинец
Cтраница 1
Потенциалы свинца исследованы в связи с образованием защитных пленок. Потенциал облагораживается при возникновении пленок и, наоборот, смещается в отрицательную сторону, когда эти пленки разрываются или растворяются с образованием комплексов. [1]
В глубокообессоленной воде потенциал свинца разблагоражива-ется до - 0 3 в и скорость коррозии значительно возрастает. [2]
С / изм - потенциал свинца, измеренный в поле блуждающих токов; ( - 0 48) - среднее значение потенциалов свинца в грунтах по сравнению с медносульфатным электродом. [3]
Окислители, потенциал которых выше потенциала свинца ( Fein / Fe 0 77 В, Hgn / Hg 0 9I В, РЬ / РЬ - 0 13В), переводят в раствор металлический свинец, но при этом весьма сильно затрагивают другие его соединения. [4]
Электродный потенциал адова очень близок к потенциалу свинца, поэтому олово практически целиком переходит в раствор и попадает в катодный свинец. [5]
Свинцевание применяется исключительно для защиты деталей от коррозии, хотя потенциал свинца менее отрицателен, чем потенциал железа, и свинцовое покрытие является катодным. Темносерый ( грязный) цвет свинцового покрытия и отсутствие блеска лишают возможности применять его для декоративных целей. Свинец обладает высокой химической стойкостью, о хорошо растворяется только в азотной кислоте; серная и соляная кислоты растворяют его только на поверхности. [6]
Электродные потенциалы меди, сурьмы, мышьяка, висмута значительно эдектроположительнее потенциала свинца, при анодном растворении эти металлы практически не должны переходить в раствор. [7]
В анодах должно быть ограничено содержание олова, так жак его потенциал близок к потенциалу свинца. [8]
В анодах должно быть ограничено содержание олова, так как его потенциал близок к потенциалу свинца. Олово растворяется из анода и выделяется на катоде вместе со свинцом; цинк и железо остаются в растворе. [9]
В анодах должно быть ограниченное содержание олова, так как его потенциал близок к потенциалу свинца. При рафинировании олово растворяется из анода и выделяется на катоде вместе со свинцом. Цинк и железо остаются в растворе. [10]
Отделение примесей при рафинировании свинца особенно затруднено потому, что многие металлы обладают равновесным потенциалом, близким к потенциалу свинца. [11]
С / изм - потенциал свинца, измеренный в поле блуждающих токов; ( - 0 48) - среднее значение потенциалов свинца в грунтах по сравнению с медносульфатным электродом. [12]
Медь перед электролизом надо удалить огневым способом, по крайней мере до 0 2 %, иначе она, не растворяясь при потенциале свинца, пассивирует аноды. Свинец, выпадающий на дно ванны при разрушении анодов, и сами аноды растворяются от действия кислорода воздуха химическим путем. [13]
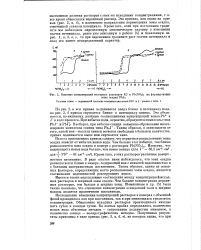 |
Влияние концентраций исходных растворов KJ и Pb ( NOs2 на формирование. [14] |
На рис. 2, а вся кривая поднимается вверх ближе к потенциалу иода, на рис. 2, б кривая спускается ближе к потенциалу свинца. Это объясняется, по-видимому, разными соотношениями концентраций ионов РЬ2г и J - в ходе процесса. Таким образом, в зависимости от того, какой ион-иод или свинец остается свободным в большем количестве, кривая поднимается выше или спускается вниз. [15]
Страницы: 1 2