Потенциал - сплав
Cтраница 4
Для того чтобы иметь возможность более полно судить о процессах, происходящих при коррозии на поверхности металла, нами было изучено изменение потенциалов сплава во STf 0 00 от держания никеля. В 0 5 % - ном растворе wau электродный потенциал сплава с увеличением содержания в нем никеля закономерно облагораживается. [46]
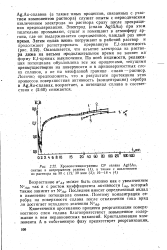 |
Хронопотенциограммы СР сплава AglSAu, снятые в непрерывном режиме ( /, а также с извлечением из раствора на 30 с ( 2. 30 мин ( 3. 16 - 18 ч ( 4. [47] |
Возрастание asAg может быть связано как с увеличением NsAg, так и с ростом коэффициента активности fAg, который также зависит от NsAg - Последнее вносит огаределенный вклад в изменение потенциала сплава. [48]
Случай, когда металлы в сплаве образуют твердый раствор характерен тем, что активность более отрицательного металла снижена ( часть его внутренней энергии связана компонентами твердого раствора) - и равновесный потенциал сплава является промежуточным между потенциалами обоих чистых металлов, потенциал сплава тем ближе к потенциалу одного из компонентов, чем больше содержание последнего в сплаве. В качестве компонентов твердого раствора могут выступать также интерметаллические химические соединения составляющих сплава. [49]
Кроме того, для повышения коррозионной стойкости легированного сплава в него дополнительно вводят так называемые катодные легирующие добавки: платину, палладий и др. ( 0 5 - 1 0 %), которые образуют на поверхности сплава мельчайшие катодные участки, вызывая анодную пассивацию и сдвигают потенциал сплава в область пассивной устойчивости. Действие катодных присадок менее благородных металлов, например, меди, молибдена и других ( 3 - 4 %), заключается в том, что они заполняют поры пассивной пленки, увеличивая ее защитное действие. [50]
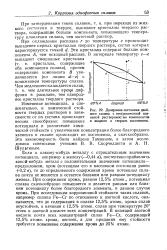 |
Диаграмма состояния двойного сплава с неограниченной взаимной растворимостью компонентов в жидком и твердом состояниях. [51] |
Если к какому-нибудь металлу с отрицательным значением потенциала, например к железу ( - 0 44 б), постепенно прибавлять какой-нибудь металл с положительным значением потенциала - предположим, хром ( потенциал его в пассивном состоянии равен 0 2 в), то до определенного содержания хрома потенциал сплава почти не меняется и остается близким или равным потенциалу железа. При содержании хрома, равном 12 5 % атомн. При исследовании коррозионной стойкости таких сплавов, например сплава Fe-Сг по отношению к азотной кислоте, оказывается, что до содержания в сплаве 12 5 % атомн. В кипящей азотной кислоте почти всех концентраций сплав Fe-Сг, содержащий 12 5 % атомн. [52]
 |
Диаграмма потенциалов же-лезоводородных сплавов. [53] |
Диаграмма потенциалов выделения / ( рис. 10) снята для осадков, полученных из горячего железного электролита, когда водород на катоде осаждается в незначительной степени. Потенциал сплава уменьшается и становится меньше потенциала исходного железа; вместе с тем микротвердость ( рис. 11) резко возрастает со 176 единиц по шкале микротвердости до 1100 единиц. [54]
Однокомпонентные сплавы, представляющие собой химические соединения или твердые растворы, ведут себя как однородные системы и переходят в раствор в том же соотношении, в котором они находятся в сплаве. Потенциал сплава в этом случае изменяется в зависимости от состава, и его значение лежит между значениями потенциалов обоих чистых металлов. [55]
Предположим, что площадь компонента А, являющегося анодом, будет больше, чем площадь компонента Б - катода. Тогда потенциал сплава будет соответствовать почти точно потенциалу А и только для сплавов, весьма близких по составу к компоненту Б, будет резко возрастать, доходя до потенциала более благородной составляющей. [56]
Если металл в щели находится в активном состоянии и коррозия протекает в области кислородной деполяризации, то уменьшение концентрации окислителя приведет к понижению скорости коррозии. Сдвиг потенциала сплава при понижении концентрации кислорода в щели в отрицательную сторону приводит к увеличению скорости растворения только в случае активации пассивного состояния. Например, как показало снятие кривых для титана ( рис. 23), в растворах NaCl при рН0 95, даже при отрицательных потенциалах, титан находится в пассивном состоянии. Было показано, что при уменьшении концентрации кислорода в зазоре ( до 0 07 мг / л) происходит сильное смещение потенциала стали 12X13 в отрицательную сторону ( до - 0 45 В), а скорость коррозии стали изменяется мало: 0 044 и 0 088 мг / ( см2 - сут) соответственно. [57]
Однако при переходе к сильно щелочным растворам наблюдается резкое возрастание скорости анодной реакции, на что указывает смещение кривых в отрицательную область потенциалов, намного больше, чем может вызывать изменение потенциала водородного электрода. Резкое смещение потенциала сплавов в положительную сторону при анодной поляризации, которое свидетельствует о переходе металла в пассивное состояние, наступает тем легче, чем ниже рН щелочного раствора. [58]
Алюминий и его сплавы исключительно чувствительны к анодной поляризации вследствие явления анодной пассивности. При сдвиге потенциала сплава выше определенного критического значения наступает пробой пленки в отдельных точках. В месте пробоя пленки идет интенсивное растворение металла с образованием коррозионной точки. Поверхность алюминиевых сплавов с повышенным содержанием меди ( Д16, АК8) в электрохимическом отношении даже после закалки изделий в холодной воде неоднородна. Потенциалы участков с пониженным содержанием меди будут более отрицательными по сравнению с остальной поверхностью сплава. На этих участках за счет анодной поляризации наступает пробой окисной пленки и возникают коррозионные точки. Потенциал коррозии сплава системы Al-Zn-Mg имеет меньшее значение, чем критический потенциал образования коррозионной точки, поэтому в обычных условиях эти сплавы не подвержены точечной коррозии. Однако коррозия сплава 52 в контакте с катодным металлом ( сталь 45), как будет показано ниже, может иметь сильно выраженный точечный характер. При анодной поляризации вследствие контакта с катодным металлом электродный потенциал смещается в область пробоя быстрее. [59]
На химическую стойкость хромистых сталей большое влияние оказывает состояние поверхности сплава. Холодная деформация снижает потенциал сплава. Наличие царапин, отдельных повреждений и участков наклепанного металла вызывает местную коррозию, которая особенно типична для хромистых сталей. [60]
Страницы: 1 2 3 4 5