Потенциал - титан
Cтраница 3
При этом, как видно из рис. 2, потенциал титана в 20 % - ной НС1 соответствует области неполной запассивированности, а в 30 % - ной HG1 титан активно растворяется. [31]
На рис. 12, а и б приведены кривые изменения потенциала титана во времени в зависимости от величины наложенного катодного тока в 40 % - ном растворе серной кислоты с добавкой J3 3 M ионов Ti4 соответственно при 20 и 100 С. [32]
 |
Коррозия меди и ее сплавов в контакте с титаном в морской воде. [33] |
В разбавленной ( 0 5 % - ной) серной кислоте потенциал титана равен 0 43 в, а потенциал алюминия равен - 0 2 в. В соответствии с этими значениями потенциалов в паре Ti - А1 анодом пары является алюминий. Коррозия алюминия вследствие этого, как видно из таблицы, возрастает. [34]
Холл и Хаккерман [88] определяли количество электричества, необходимое для изменения потенциала титана в растворе хлорида натрия до потенциала выделения кислорода. Они пришли к заключению, что при этом образуется от одного до пяти монослоев TiCb, Однако есть основание полагать, что в действительности образующийся ТЮ2 залечивает уже существующую начальную окисную пленку. Кабанов, Бурштейн и Фрум-кин [89] отмечают, что анодная пассивация железа в щелочном растворе сильно зависит от степени окисленности исходной поверхности. [35]
Холл и Хаккерман [88] определяли количество электричества, необходимое для изменения потенциала титана в растворе хлорида натрия до потенциала выделения кислорода. Они пришли к заключению, что при этом образуется от одного до пяти монослоев Ti02i Однако есть основание полагать, что в действительности образующийся TiO2 залечивает уже существующую начальную окисную пленку. Кабанов, Бурштейн и Фрум-кин [89] отмечают, что анодная пассивация железа в щелочном растворе сильно зависит от степени окисленности исходной поверхности. [36]
Присутствие в рафинируемом металле примесей с потенциалом, близким к величине потенциала титана, приводит к их совместному растворению на аноде и выделению на катоде. [37]
Таким образом, революционер оказывается сакральным оператором, который делает социально реальным мифологический потенциал титана и героя. [38]
NaOH, 6 % - ной HNO3, соприкасающимися с воздухом, титан возобновляет пассивное состояние, так как потенциал титана нисле зачистки поверхности снова возвращается к значениям, отвечающим пассивному состоянию ( см. фиг. [39]
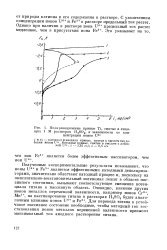 |
Поляризационные кривые Ti, снятые в кипящих 1 М растворах H2S04, в зависимости от концентрации ионов U6 1. [40] |
Полученные экспериментальные результаты показывают, что ионы U6 и Fe3 являются эффективными катодными деполяризаторами, значительно облегчают катодный процесс и, поскольку их окислительно-восстановительный потенциал лежит в области пассивного состояния, вызывают соответствующее смещение потенциала титана в пассивную область. Для перевода титана в устойчивое пассивное состояние необходимо, чтобы катодный ток восстановления ионов металлов переменной валентности превысил максимальный ток анодного растворения титана. [41]
Важнейшими электрохимическими показателями, определяющими возможность осаждения титана на катоде, являются: величина стандартного потенциала, или положение металла в ряду напряжений, и величина перенапряжения водорода. Станцартный потенциал титана Е0, рассчитанный Боттсом и Краускопфом [2] по результатам измерения потенциалов в 0 25 М растворах Т12 ( 8С4) з и TiCla, составляет в первом случае - 0, 168 и во втором - 0, 218 вольта. Стандартный потенциа лсистемы Ti3 Ti, рассчитанный Сато и Ямане [3] по экспериментальным данным, равен - 0 355 вольта. [42]
В щелочных, нейтральных и кислых окислительных средах, а также в разбавленных восстановительных кислотах при анодной поляризации титана не происходит активного анодного растворения, характерного для железа и других металлов, а также и для титана кислых восстановительных средах. При анодной поляризации потенциал титана сразу же смещается в положительную сторону до величины, соответствующей какой-то другой возможной электрохимической реакции ( выделение С12, 02) в зависимости от состава электролита, плотности тока и других факторов. [43]
В большинстве сред потенциалы титана, сплава Монель и нержавеющей стали в пассивном состоянии примерно одинаковы, и поэтому при соединении этих металлов электрохимические эффекты не возникают. Если титан и находящийся с ним в контакте материал являются разнородными металлами, то ти-тан обычно играет роль эффективного катода, и хотя к значительной коррозии титана такой контакт скорее всего не приведет, отрицательное воздействие на второй металл окажет. [44]
В щелочных, нейтральных и кислых окислительных средах, а также в разбавленных восстановительных кислотах при анодной поляризации титана не происходит активного анодного растворения, характерного для железа и других металлов, а также и для титана в кислых восстановительных средах. При анодной поляризации потенциал титана сразу же смещается в положительную сторону до величины, соответствующей какой-то другой возможной электрохимической реакции ( выделение С12, 02) в зависимости от состава электролита, плотности тока и других факторов. [45]
Страницы: 1 2 3 4 5