Приложенный потенциал
Cтраница 1
 |
Вольт-амперная ячейка с капель. [1] |
Приложенный потенциал откладывают на оси абсцисс. На рисунке показаны две шкалы, относящиеся к нормальному водородному и к насыщенному каломельному электродам. Переход от одного электрода сравнения к другому требует только изменения положения точки, соответствующей нулевому потенциалу. В полярографии в качестве электрода сравнения чаще всего применяется НасКЭ - Как видно из рис. 49, принято откладывать увеличивающиеся значения отрицательных потенциалов направо. [2]
 |
Вольт-амперная ячейка с капельным ртутным катодом и ртутным анодом. [3] |
Приложенный потенциал откладывают на оси абсцисс. На рисунке показаны две шкалы, относящиеся к нормальному водородному и к насыщенному каломельному электродам. Переход от одного электрода сравнения к другому требует только изменения положения точки, соответствующей нулевому цотенциалу. Как видно из рис. 49, принято откладывать увеличивающиеся значения отрицательных потенциалов направо. Если значение потенциала находится в области, лежащей вправо от нулевого потенциала относительно НВЭ, говорят, что микроэлектрод поляризован отрицательно, если влево-поляризован положительно. [4]
Приложенный потенциал, вероятно, оказывает некоторое воздействие на коэффициент / С и, таким образом, оказывает вторичное влияние на константу скорости. [5]
Поскольку приложенный потенциал слишком низок для окисления цианид-иона, то первоначальной реакцией будет окисление субстрата, приводящее к образованию катион-радикала. Последующие стадии включают присоединение цианид-иона, перенос второго электрона и потерю протона, однако не ясно, в какой момент времени происходит атака цианид-ионом. [6]
 |
Кривая титрования при амперометрическодо титровании. [7] |
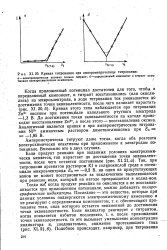
Когда приложенный потенциал достаточен для того, чтобы и определяемый компонент, и титрант восстановились ( или окислились) на микроэлектроде, в ходе титрования ток уменьшается до достижения точки эквивалентности, после чего начинает нарастать ( рис. XI. Кривая этого типа наблюдается при титровании Zn2 оксином при потенциале капельного ртутного электрода - 1 3 В. До достижения точки эквивалентности на катоде проис-ходит восстановление Zn2, а после этого - восстановление оксина. Аналогичной является кривая и при амперометрическом титровании Ni2 аммиачным раствором диметилглиоксима при ЕЬ - 1 85 В. [8]
Если приложенный потенциал имеет достаточно большое значение, одни электроактивные частицы восстанавливаются на катоде, другие окисляются на аноде. Такой электролитический процесс приводит к появлению в цепи электрического тока. [9]
Величина приложенного потенциала ограничен. Попадая в пространство между острием и стенкой, ионизирующая частица вызывает разряд; сопротивление ft ограничивает ток и таким обпааом rfefcf разряд. Число разрядов подсчитывается, например, с помощью регистрирующего приспособления ( усилитель и телефон), индуктивно связанного со счетчиком по току, или, как на чертеже, с помощью струйного электрометра. [10]
Если величина приложенного потенциала составляет около 20000 в Iсм, ион движется со скоростью около 1 м сек, и, таким образом, за время релаксации он проходит путь, в несколько раз превышающий толщину эффективной ионной атмосферы. В результате движущийся ион фактически свободен от ионной атмосферы противоположного знака, так. В этих условиях как релаксационный, так и электрофоретический эффекты сильно уменьшаются и при достаточно высоких напряжениях должны исчезнуть. В этом случае эквивалентная электропроводность при любой конечной концентрации должна быть больше, чем соответствующее значение при низких напряжениях. Увеличение электропроводности электролита при высоких градиентах потенциала наблюдалось Вином [14] до того, как была дана какая-либо теоретическая интерпретация этого явления, поэтому оно известно под лазванием эффекта Вина. [11]
В точке А приложенный потенциал равен нулю, поэтому при прямом и обратном смещениях расстояния ОА и 0В сохраняются такими же, как и в состоянии равновесия. [12]
Индифферентный электролит и приложенный потенциал влияют на константу скорости только через т ] и срр. [13]
 |
Электролизер простой конструкции. [14] |
При повышении величины приложенного потенциала от нуля и выше ток по существу не будет протекать до тех пор, пока не будет достигнут потенциал разложения. [15]
Страницы: 1 2 3 4 5