Вертикальный потенциал - ионизация
Cтраница 2
Вертикальный потенциал ионизации будет равен 26 7, но этот уровень лежит примерно на 2 5 - 3 эв выше предела диссоциации, поэтому распад будет сопровождаться избытком энергии такого же порядка. Кривая производной позволяет с большой чувствительностью обнаружить эту избыточную энергию. [16]
Они определяют вертикальные потенциалы ионизации исходной мол. Орбитальные энергии широко используются при интерпретации фото - и рентгеноэлектронных спектров, в к-рых каждая полоса примерно отвечает потенциалу ионизации при удалении электрона с той или иной мол. Орбитали ф, получаемые при решении ур-ний Хартри-Фока, обычно наз. Те же, к-рые не используются при конструировании волновой ф-ции данного состояния системы, наз. [17]
Обычно говорят, что эта энергия равна вертикальному потенциалу ионизации молекулы, который больше адиабатического на величину энергии колебательного возбуждения иона. Так, вертикальный потенциал ионизации водорода близок к 16 0 эв. [18]
Кажется очевидным, что вертикальный потенциал ионизации будет выше адиабатического потенциала ( энергии, необходимой для перехода О-О) на некоторую величину, которая зависит от степени структурных изменений, вызванных отрывом электрона. Поэтому вопрос о том, какой электрон вырывается из молекулы ( связывающий, несвязывающий или обусловливающий состояние отталкивания ядер), приобретет решающую роль при определении величины разности этих двух потенциалов. [19]
В последнем случае перенос электрона приведет к неравновесному состоянию координационной сферы, так как обычно перенос электрона происходит без изменения межъядерного расстояния. В этом случае при расчетах необходимо учитывать вертикальные потенциалы ионизации и сродство к электрону соответственно. [20]
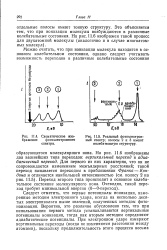 |
Схематическое изображение фотоэлектронного спектра.| Реальный фотоэлектронный спектр. полосы 2 и 3 имеют колебательную структуру. [21] |
Следует отметить, что первые потенциалы ионизации, измеренные методом электронного удара, всегда на несколько десятых электронвольта выше значений, полученных методом фотоионизации. Вероятно, это различие обусловлено тем, что при использовании первого метода устанавливаются вертикальные потенциалы ионизации, тогда как вторым методом определяют адиабатические потенциалы. [22]
При ионизации различных молекул RiR2 могут встретиться следующие три случая. В первом из них, когда кривые потенциальной энергии молекулы и иона имеют минимумы на одинаковых равновесных расстояниях, вертикальный потенциал ионизации совпадает с адиабатическим. Во втором случае, когда минимум кривой потенциальной энергии она находится при несколько большем равновесном расстоянии, вертикальный потенциал ионизации будет больше адиабатического; хвост кривой появления ионов достигает, однако, адиабатического потенциала ионизации. В третьем случае, когда потенциальные кривые молекулы и иона сдвинуты одна относительно другой так сильно, что наиболее вероятные переходы происходят на очень высокие уровни, вертикальный ( измеренный) потенциал ионизации может очень сильно превысить адиабатический. [23]
 |
Виды колебательной структуры. [24] |
Структура I появляется при ионизации несвязывакмцето ( или слабосвязывающего, слаборазрыхляющего) электрона. При удалении несвязывающего электрона межъядерные расстояния значительно не изменяются, поэтому в соответствии с принципом Франка - Кондона ( см. § 1) наблюдается с достаточной интенсивностью только один переход, соответствующий вертикальному потенциалу ионизации. Для этого перехода, как пояснялось в § 1, значение вертикального потенциала близко к адиабатическому. [25]
При использовании бомбардировки электронами следует проводить различие между понятиями вертикального потенциала ионизации и потенциала ионизации, который можно было бы назвать минимальным. Поэтому если энергия электронов такова, что ток ионов А максимален, то электрон может удалиться от М настолько быстро, что А и В не успеют разойтись и в результате последующего разделения А и В приобретут заметную кинетическую энергию. Вертикальный потенциал ионизации отличается от минимального потенциала, требуемого для образования А и В, на величину полной кинетической энергии, сообщаемой осколкам молекул. [26]
 |
Начальные участки кривых ионизации для исследуемого объекта и стандартного вещества ( например, Аг. [27] |
Потенциал ионизации, соответствующий переходу с нулевого колебательного уровня молекулы на нулевой колебательный уровень основного электронного состояния иона, называется адиабатическим потенциалом ионизации. В эксперименте при ионизации электронным ударом в основном осуществляется вертикальный переход на верхние колебательные уровни с образованием возбужденного иона. Следовательно, измерения приводят не к адиабатическим, а к вертикальным потенциалам ионизации, которые всегда больше первых. Задача экспериментатора - приблизить условия ионизации к адиабатическим. [28]
При ионизации различных молекул RiR2 могут встретиться следующие три случая. В первом из них, когда кривые потенциальной энергии молекулы и иона имеют минимумы на одинаковых равновесных расстояниях, вертикальный потенциал ионизации совпадает с адиабатическим. Во втором случае, когда минимум кривой потенциальной энергии она находится при несколько большем равновесном расстоянии, вертикальный потенциал ионизации будет больше адиабатического; хвост кривой появления ионов достигает, однако, адиабатического потенциала ионизации. В третьем случае, когда потенциальные кривые молекулы и иона сдвинуты одна относительно другой так сильно, что наиболее вероятные переходы происходят на очень высокие уровни, вертикальный ( измеренный) потенциал ионизации может очень сильно превысить адиабатический. [29]
Чтобы оценить величину АЕ, которая относится к действительному переносу электрона, необходимо учесть принцип Франка - Кондона. В результате этого для одноатомных ионов первый член выражения (4.34) остается неизменным. Для двухатомных или многоатомных ионов или молекул это не соблюдается, так как для этих случаев в уравнение (4.34) необходимо подставлять вертикальный потенциал ионизации или сродство к электрону соответственно. Это связано с тем, что только те электронные переходы, которые не сопровождаются изменением межъядерных расстояний, происходят с большой вероятностью. Подобная в некотором отношении ситуация наблюдается и для второго члена уравнения (4.34), связанного с сольватацией ( AS), так как опять-таки на основе принципа Франка - Кондона ориентация молекул воды остается практически неизменной за время переноса электрона. [30]
Страницы: 1 2