Реальный потенциал
Cтраница 2
Реальные потенциалы окислительно-восстановительных систем с аналитической точки зрения более ценны, чем стандартные потенциалы, так как истинное поведение системы определяется не стандартным, а реальным потенциалом и именно последний позволяет предвидеть протекание окислительно-восстановительной реакции в конкретных условиях. [16]
Реальным потенциалом называется потенциал электрода ( относительно стандартного водородного электрода), а котором происходит интересующая нас полуреакция в заданном растворе электролита, когда формульные концентрации и окислителя, и восстановителя равны единице. [17]
Однако реальный потенциал этой полуреакции равен 1 00 В в 1 F растворе хлористоводородной кислоты и 1 11 В в 2 F растворе серной кислоты. [18]
Такой реальный потенциал окислительно-восстановительного электрода в нормальных условиях называют формальным потенциалом. [19]
Но реальный потенциал реакции восстановления нитрата может несколько отличаться от приведенных значений, поскольку на кинетику этой катодной реакции сложное влияние оказывают продукты реакции и кислород. [20]
Значение реального потенциала зависит также от потенциала жидкостного соединения, возникающего между электродом сравнения и исследуемым полуэлемснгом. [21]
Величина реального потенциала зависит от присутствующих в растворе веществ и в большинстве случаев может быть определена только экспериментально. [22]
Знание реальных потенциалов необходимо для решения вопроса о направлении окислительно-восстановительного процесса и ходе потенциометр ического титрования. [23]
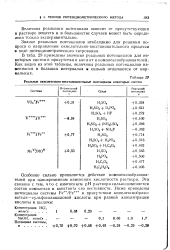 |
Реальные окислительно-восстановительные потенциалы некоторых систем. [24] |
Величина реального потенциала зависит от присутствующих в растворе веществ и в большинстве случаев может быть определена только экспериментально. [25]
Знание реальных потенциалов необходимо для решения вопроса о направлении окислительно-восстановительного процесса в ходе потенциометрического титрования. [26]
Величина реального потенциала зависит от присутствующих в растворе веществ и в большинстве случаев может быть определена только экспериментально. [27]
 |
Реальные окислительно-восстановительные потенциалы некоторых систем. [28] |
Величина реального потенциала в большинстве случаев может быть определена только экспериментально. [29]
Величина реального потенциала зависит также от потенциала жидкостного соединения, возникающего между электродом сравнения, применяемым при измерениях, и исследуемым полуэлементом. [30]
Страницы: 1 2 3 4