Стационарный потенциал - сталь
Cтраница 3
Деаэрация растворов уксусной кислоты, как это было показано, приводит к сдвигу стационарного потенциала сталей в отрицательную сторону. В случае аустенитных сталей это неопасно. [31]
Рост концентрации хлорида в систеуе хлористый НЕ трии - вода аномально сказывается и на изменении стационарного потенциала стали. Повышение концентрации хлорида от 0 07 % до 1 % сдвигает стационарный потенциал стали к менее положительным значзнияа. При этом замедляется и скорость растворения стали. Дальнейшее поркшение концентрации хлорида приводит к значительному смещению стационарного потенциала стали в сторону отрицательных значений, и скорость растворения стала еще более замедляется. Наконец, при концентрациях хлорида выше 20 % потенциал не зависит от содержания хлорида. Этой независимости потенциала от концентрации хлорида соответствует инициальная скорость расгвирзния сгали ( кр. [32]
Следует отметить, что при деаэрации раствора вследствие удаления деполяризатора - кислорода - происходит сдвиг стационарного потенциала стали IX17H2 в отрицательную сторону на - 300 мв. Стационарный потенциал стали 1Х17Ш в деаэрированном растворе устанавливается очень близко к границе пассивной области ( Фладе-потенциалу), сталь продолжает оставаться в пассивном состоянии. [33]
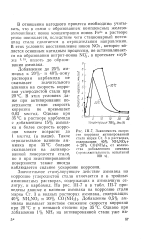 |
Зависимость скорости коррозии активированной стали марки Ст. 3 в растворах, содержащих 40 % NH4NO3 20 % CO ( NH2 2, от количества добавленного аммиака ( продолжительность испытаний 100 ч. [34] |
В отношении катодного процесса необходимо учитывать, что в связи с образованием комплексных железо-аммонийных ионов концентрация ионов Fe2 в растворе резко понижается, вследствие чего стационарный потенциал стали сдвигается в отрицательном направлении. В этих условиях восстановление ионов NOs, которое является основным катодным процессом, не останавливается на образовании нитрит-ионов N02, а протекает глубже 9 15, вплоть до образования аммиака. [35]
Особенности процесса МКК в условиях эксплуатации ( скорость коррозии, характер ее изменения и механизм процесса) будут определяться тем, в какой из областей находится стационарный потенциал стали. [36]
Таким образом, механизм коррозии стали в бетоне в воздушно-сухих условиях проходит по пути окисления ( на конечной фазе) с образованием у - FeOOH, составляющую основу для образования пассивной пленки значения стационарных потенциалов стали стремятся к - 0 1В по х.с.э. В случае насыщения бетонов пластовой водой механизм окисления по первым двум валентностям остается неизменным. Но в силу того, что ионы хлора [5] нарушают пассивацию, появляется возможность для образования гидроокиси железа, что приводит к резкому уменьшению потенциала стали и резкому увеличении скорости коррозии. [37]
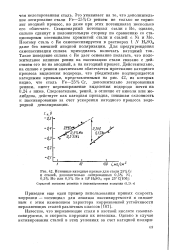 |
Истинные катодные кривые для стали 25 % Сг и сталей, дополнительно легированных 0 5 % Ni, 0 5 % Мо или 0 5 % Re в 1JV H2S04 при 25 С. [38] |
Это указывает на то, что дополнительное легирование стали Fe-25 % Сг рением не только не тормозит анодный процесс, но даже при этих потенциалах несколько его облегчает. Стационарный потенциал стали с Re, однако, сильно сдвинут в положительную сторону по сравнению со стационарным потенциалом хромистой стали и сталей с Ni и Мо. Поэтому сталь с Re самопассивируется в растворах 1 N H2S04 даже без внешней анодной поляризации. [39]
Критериями электрохимической защиты являются защитный потенциал и защитная плотность тока. Стационарный потенциал стали в природных коррозионных средах в среднем составляет 0 440 В. В табл. 9.8 и 9.9 приведены значения защитных потенциалов некоторых металлов в природных коррозионных средах и необходимая плотность тока с учетом состояния покрытия. Наиболее часто используется контроль по значениям потенциалов. Плотность тока в процессе эксплуатации может меняться из-за нарушения изоляции защищаемой конструкции ( при совместном применении) и из-за образования на катодных поверхностях ме-таллоосадков. [40]
Следует отметить, что при деаэрации раствора вследствие удаления деполяризатора - кислорода - происходит сдвиг стационарного потенциала стали IX17H2 в отрицательную сторону на - 300 мв. Стационарный потенциал стали 1Х17Ш в деаэрированном растворе устанавливается очень близко к границе пассивной области ( Фладе-потенциалу), сталь продолжает оставаться в пассивном состоянии. [41]
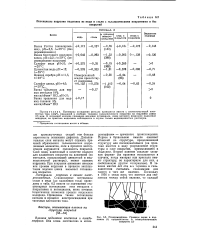 |
Псевдоморфизм. Границы зерен в подложке ( / продолжаются в электролитическое покрытие ( 2. [42] |
Стационарные потенциалы стали и меди ( до наложения тока) приведены в табл. 6.2 вместе со значениями стационарных потенциалов этих металлов с покрытиями и потенциалов, ниже которых теоретически возможен процесс выделения водорода. Приведены также потенциалы катодов в процессе электроосаждения при типичных плотностях тока. [43]
 |
Компенсационная схема. [44] |
При этом могут быть использованы микроамперметры М-109 и М-132 и ампервольтметры М-231. Стационарный потенциал стали относительно медно-сульфатного электрода компенсируется включением в измерительную цепь встречной ЭДС источника постоянного тока. В качестве такого источника используется батарея 1 6 - ФМЦ-У-32 с рабочим напряжением 1 6 В. [45]
Страницы: 1 2 3 4 5