Замена - аминокислота
Cтраница 1
Замена аминокислоты может иметь место как в а -, так и в р-щепи. Аномальные гемоглобины [53], получающиеся в результате этой замены, отличаются от Hb А поведением при электрофорезе и хроматографии на карбоксиметилцеллюлозе и могут быть таким образом идентифицированы и выделены. [1]
Замена аминокислоты L-ряда на аминокислоту D-ряда или замена даже одной L-аминокислоты на другую может привести к полному исчезновению биологической активности пептида. [2]
Если замены аминокислот, вставки и делении представляются сравнительно небольшими структурными модификациями в ходе эволюции, то процесс слияния генов вызывает очень существенные изменения: он приводит либо к объединению друг с другом разных полипептидных цепей, либо к дупликации данной цепи. [3]
Влияние замен аминокислот во внутренней части белка часто компенсируется другими заменами. [4]
Сходным образом, замены аминокислот в дефектных молекулах гемоглобина ( рис. 4 - 17) в большинстве случаев могут быть обусловлены изменением только одного основания. [5]
Мы еще не знаем, какого рода замены аминокислот должны происходить, чтобы зависимость / См от температуры изменилась. [6]
 |
Влияние некоторых гипотетических точковых мутаций замещения на биологическую активность конечного белкового продукта. [7] |
Может также случиться, что, несмотря на происшедшую замену аминокислоты, мутантный белок сохранит способность выполнять свою функцию, но будет отличаться от нормального белка по своим свойствам и потому окажется не столь эффективным, как нормальный белок. [8]
Ценные результаты получены методом сайт-специфичного мутагенеза, основанного на направленной замене аминокислот в белковой молекуле методами генетической инженерии. [9]
Замены аминокислот по отношению к р - МСГ человека обозначены горизонтальной чертой. [10]
В НЬМ гистидин заменен на тирозин, в результате НЬМ стабилизирован в форме метгемоглобина и не способен связывать кислород. Замена аминокислоты во внутренней части молекулы гемоглобина приводит к изменению третичной структуры и как следствие - к нестабильности молекулы НЬ. [11]
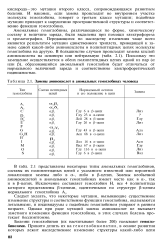 |
Замены аминокислот в аномальных гемоглобинах человека. [12] |
Следует указать, что некоторые мутации, вызывающие существенное изменение структуры и соответственно функции гемоглобина, оказываются летальными, и индивидуумы с подобным гемоглобином умирают в раннем возрасте. Однако при ряде мутаций замена аминокислот не вызывает заметного изменения функции гемоглобина, в этих случаях болезнь протекает бессимптомно. [13]
Одна из причин этого - большая изменчивость вирусов. Вирусы часто мутируют, в их белках происходят отдельные замены аминокислот и старые антитела уже не узнают эти белки. В результате вакцинацию приходится проводить вновь и вновь. [14]
Корреляция выдерживается, хотя в каждом конкретном случае замены аминокислот находятся под сильным давлением отбора. Отметим, что корреляция, приведенная на рис. 9.1, б, пока еще никак не объяснена. [15]
Страницы: 1 2 3