Более отрицательный потенциал
Cтраница 1
 |
Анодная поляризация и коррозия. [1] |
Более отрицательные потенциалы приводят к защелачива-нию раствора вблизи поверхности свинца, что вызывает его растворение. Свинец, находящийся в почве, образует РЬ РЬ2 - электрод. [2]
Более отрицательные потенциалы Енп и Епп и малые критические токи пассивации способствуют тому, что титан легко пассивируется во многих кислых средах. [3]
Имея более отрицательные потенциалы, чем амальгамы щелочных металлов, амальгамы тетраалкилзамещенных аммония являются весьма энергичными восстановителями. Однако их восстановительная способность в исследованиях и в химических технологиях используется мало. [4]
Имея более отрицательный потенциал, чем железо, цинковое покрытие является анодом по отношению к железу и таким образом защищает сталь от коррозии электрохимически. При этом в образующейся гальванической паре цинк - железо цинковое покрытие подвергается растворению с образованием продуктов коррозии. Поэтому металл основы не подвергается коррозии. [5]
При более отрицательных потенциалах ( меньше - 0 56 в) ртуть заряжена отрицательно и максимумы называются отрицательными. [6]
При более отрицательных потенциалах в апротонных растворителях была получена вторая полярографическая волна восстановления кислорода, причем этот потенциал полуволны зависел от природы катиона фонового электролита. Было предположено, что продуктом восстановления при потенциалах второй волны является пероксидный ион. [7]
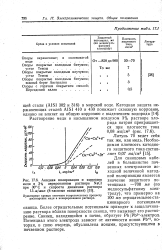
При более отрицательных потенциалах, чем ф вн, кривая k z изображает суммарный ток, обусловленный двумя катодными реакциями: i2 io2 JH I причем io2 & пред. Естественно, что положение поляризационных кривых и характерных точек на диаграмме зависит от природы рассматриваемой системы. [8]
При более отрицательных потенциалах, чем Ф евн, окисление металла прекращается и остаются только реакции восстановления двух окислителей. [9]
При более отрицательных потенциалах ( участок б) скорость процесса увеличивается, что связано с восстановлением другого окислителя. Например, на первых двух участках ( а, б) происходит восстановление кислорода, а на участке в - восстановление водорода из молекул воды в нейтральных или ионов Н3О в кислых средах. [10]
При более отрицательных потенциалах присоединяется второй электрон ( путь III) И дианион протонируется. Часто вторая волна соответствует переносу более чем одного электрона. Это означает, что R3 имеет более высокое сродство к протону и успевает протонироваться вблизи электрода. [11]
При более отрицательных потенциалах присоединяется второй электрон ( путь III) и дианион протонируется. Часто вторая волна соответствует переносу более чем одного электрона. Это означает, что R2 - имеет более высокое сродство к протону и успевает протонироваться вблизи электрода. [12]
При более отрицательных потенциалах может происходить частичное десульфирование. [13]
 |
Зависимость lg i от lg т ( по данным 5 при. - 1 0 ( 1 и. - 1 5 в ( 2. [14] |
При более отрицательном потенциале ( - 1 5 в) зависимости i от т следующие: i - T - 3 при малых т и i - т при больших тг И здесь эти зависимости можно трактовать как результат наложения диффузии, кинетики и адсорбции. Аналогичная зависимость получается при потенциалах положительнее потенциала максимального ингибирования, например при - 0 4 в. При самых коротких периодах капания в спирто-водных растворах на таст-поляро-граммах наблюдается максимум в катодной области потенциалов. [15]
Страницы: 1 2 3 4