Первый потенциал
Cтраница 2
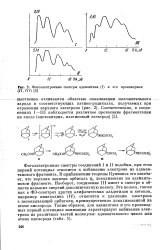 |
Фотоэлектронные спектры адамантана ( / и его производных. [16] |
Фотоэлектронные спектры соединений I и II подобны, при этом первый потенциал относится к выбиванию электрона из адаман-танового фрагмента. В приближении теоремы Купманса это означает, что верхняя занятая орбиталь % локализована на адаманта-новом фрагменте. Наоборот, соединение III имеет в спектре в области меньших энергий дополнительную полосу. Эта полоса, также как в ФЭ-спектрах других алифатических альдегидов и кетонов, например пинаколина ( IV), относится к удалению электрона с несвязывающей орбитали, преимущественно локализованной на атоме кислорода. [17]
 |
Схема строения коллоидных мицелл кремнезоля и их взаимодействие со шлаком. [18] |
Действие этих сил вызывает избирательное присоединение из раствора гидроксильных ионов - ОН, которые образуют первый потенциал оопределяющий слой мицеллы кремнезоля. В связи с этим частицы приобретают отрицательный заряд, действие которого вызывает группировку вокруг частицы положительно заряженных ионов, образующих второй электрический так называемый диффузионный слой мицеллы. Потенциалоопределяющим ионом диффузионного слоя в мицеллах кремнезоля жидкого стекла является ион натрия Na, способный удерживать вокруг себя до нескольких слоев поляризованных водных молекул. [19]
Как видно из табл. 13, приведенный третий и второй потенциалы для 45-электронов близки по величине друг к другу, а первый потенциал, принадлежащий более наружному 4р - электрону, отличается от них; ход значений потенциала по III группе немонотонен. Так, In имеет первый потенциал, меньший по величине, чем Ga или Т1 примерно на 0 2 - 0 3 эв. Для р-потен-циала эта разница в 4 раза больше, а именно 0 02 - 0 3 эв. Для s - потенциала эта разница в 4 раза больше, а именно около 0 8 эв. [20]
Изучение продуктов восстановления бензофенона на ртутном катоде при потенциалах, лежащих между-1 06 и-1 30 в, показало, что при первом потенциале основным продуктом восстановления является бензопинакон, в то время как при более отрицательных потенциалах образуется дифенилкарбинол. [21]
Функционал ( 207) иногда называют эффективным действием, но мы предпочтем термин первое преобразование Лежандра, имея в виду преобразование по первому потенциалу. Более сложные преобразования рассматриваются в гл. [22]
Потенциалы ионизации в первом ряду переходных металлов ( от скандия до меди) изменяются, в сравнительно узких пределах ( от 6 54 В у скандия до 7 86В у кобальта), причем в этом интервале нет четкой зависимости между порядковым номером и величиной потенциала. Первый потенциал меди довольно велик ( 7 72 В), но особенно значителен третий потенциал ионизации меди ( 36 8В), почти такси же потенциал у никеля. Поэтому перевод этих атомов в трехзарядное состояние затруднителен. [23]
Как изменяется первый потенциал ионизадии с ростом порядкового номера элементов в главной и побочной подгруппах. [24]
Такая же величина обнаруживается и при съемке кривых в потоке азота. Предельный ток после первого потенциала обусловлен предельной скоростью доставки растворяющегося газа к месту реакции. В нашем случае величина предельного тока мало зависит от скорости потока газа мимо электрода и, таким образом, лимитирующей стадией подачи газа являются сорбционные процессы и поверхностная диффузия газов на электроде. [25]
Поэтому говорит о первом потенциале и о н и з а п, и и ( энергия отрыв. По мере нсдл / ь П ггельного удаления электронов от атома, положительный з - 1рнд обра. [26]
Как видно из табл. 13, приведенный третий и второй потенциалы для 45-электронов близки по величине друг к другу, а первый потенциал, принадлежащий более наружному 4р - электрону, отличается от них; ход значений потенциала по III группе немонотонен. Так, In имеет первый потенциал, меньший по величине, чем Ga или Т1 примерно на 0 2 - 0 3 эв. Для р-потен-циала эта разница в 4 раза больше, а именно 0 02 - 0 3 эв. Для s - потенциала эта разница в 4 раза больше, а именно около 0 8 эв. [27]
В работе [224] методом фотоионизационной масс-спектромет-рии определены потенциалы ионизации некоторых нитроксилов. Для 2 2 6 6-тетраметилпиперидин - 1-оксила первый потенциал ( 6 91 эВ) связан с образованием катиона в основном синглетном состоянии, а верхние потенциалы ( 8 64 и 9 3 эВ) - с образованием катиона в триплетном и синглетном возбужденных состояниях. [28]
 |
Электролитическая ячейка для измерения потенциалов разложения. [29] |
Однако / - F-кривые для системы SnCb - KCI - FeCb, снятые без предварительного электролиза, имеют два излома. Очевидно, соответствующие им потенциалы отвечают выделению олова ( первый потенциал) и затем железа. [30]
Страницы: 1 2 3