Первый потенциал - ионизация
Cтраница 2
Первый потенциал ионизации бора, 8 296 эв, довольно высок, а следующие два еще выше. Поэтому общая энергия, требуемая для получения ионов В3, гораздо больше, чем можно было бы скомпенсировать энергией решетки ионных соединений или гидратацией таких ионов в растворе. Следовательно, простая потеря электрона с образованием катиона не играет никакой роли в химии бора. Вместо этого решающее значение имеет образование ковалентной связи, ввиду чего соединения бора по своим свойствам и реакциям обычно похожи на соединения других неметаллов, особенно кремния. [16]
Первый потенциал ионизации атомарного водорода равен 13 54 В. [17]
Первый потенциал ионизации молекулы бензола равен 9 21 эв II ] или 212 ккал / моль. Поскольку a Р - 212 ккал / моль, а р - 18 ккал / моль, для кулонов-ского интеграла а получаем значение, равное - 194 ккал / моль. [18]
Близость первых потенциалов ионизации тризтилборана и три-винилборана уже отмечалась в разд. Сделанный из этого вывод об отсутствии я-связывания в тривинилборане [21] противоречит, однако, всем другим физическим данным ( включая данные по дифракции электронов, свидетельствующие о планар-ности молекулы [47]), и является слишком упрощенным. [19]
Близость первых потенциалов ионизации триэтилборана и три-винилборана уже отмечалась в разд. Сделанный из этого вывод об отсутствии л-связывания в тривинилборане [21] противоречит, однако, всем другим физическим данным ( включая данные по дифракции электронов, свидетельствующие о планар-ности молекулы [47]), и является слишком упрощенным. [20]
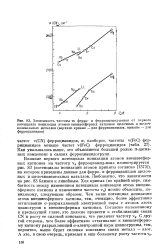
Влияние первого потенциала ионизации атомов внешнесферных катионов на частоту ve ферроцианид-иона иллюстрируется рис. 83 ( потенциалы ионизации атомов приняты согласно [1373]), на котором приведены данные для ферро - и феррицианидов щелочных и щелочноземельных маталлов. Любопытно, что зависимости на рис. 83 близки к линейным. [22]
Сначала рассмотрим первые потенциалы ионизации для каждого атома: Li 124 ккал / моль; Н 313 6 ккал / моль и F 402 ккал / моль. Водород удерживает свой валентный электрон прочнее, чем литий, но еще прочнее удерживает валентный электрон фтор. Если водород может оттягивать к себе электроны в LiH, то в HF фтор должен оттягивать электроны от атома водорода. [23]
Тион - первый потенциал ионизации ц, - приведенная масса электронов и ионов, h, k - постоян ные Планка и Больцмана, 2а, zt - соответственно статисти ческие суммы атома и иона. [24]
По оценкам первый потенциал ионизации XeF2 равен 11 5 ОД эв по сравнению с потенциалом ионизации ксенона, равным 12 12 эв. Отчасти различие между этими величинами может быть приписано влиянию я-связи. Однако рассчитанная энергия орбитали весьма чувствительна к выбору параметров, и поэтому степени согласия с экспериментами не следует придавать слишком большого значения. [25]
Так, первый потенциал ионизации лития составляет 632 кДж / моль, а бериллия - 899 кДж / моль ( ср. [26]
Здесь приведены только первые потенциалы ионизации соединении. Большой интерес для выяснения электронного строения соединений представляет также исследование их более высоких потенциалов ионизации, которое выполняется методом фотоэлектронной спектроскопии. Этот метод, предложенный почти одновременно А. Аль-Джобури в Англии ( 1961 - 1962 гг.), бурно развивается в настоящее время. [27]
Между величиной первого потенциала ионизации и реакционной способностью газообразных атомов элемента должна существовать тесная связь. Читателю предоставляется возможность в качестве упражнения установить эту связь и объяснить наблюдаемые вместе с тем отклонения от найденной закономерности. [28]
В рассматриваемом случае первый потенциал ионизации ( при 15 6 эВ) соответствует слабо связывающей, второй ( при 16 9 эВ) - сильно связывающей и третий ( при 18 8 эВ) - слабо разрыхляющей орбиталям соответственно. [29]
Теплота атомизации и первый потенциал ионизации для серебра составляют 66 и 174 ккал / моль соответственно. I приведены значения энергий связи для галогенов. Теплота испарения брома составляет 8 ккал / моль, а теплота сублимации иода - 15 ккал / моль. [30]
Страницы: 1 2 3 4