Равновесный окислительно-восстановительный потенциал
Cтраница 1
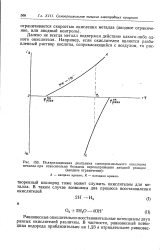 |
Поляризационная диаграмма самопроизвольного окисления. [1] |
Равновесные окислительно-восстановительные потенциалы двух разных окислителей различны. [2]
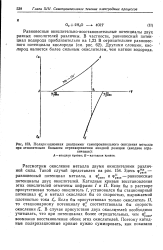 |
Поляризационная диаграмма самопроизвольного окисления металла при относительно большом перенапряжении анодной реакции ( анодное ограничение. Л - анодная кривая. / С-катодная кривая. [3] |
Равновесные окислительно-восстановительные потенциалы двух разных окислителей различны. Другими словами, кислород является более сильным окислителем, чем катион водорода. [4]
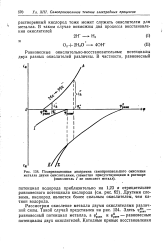 |
Поляризационная диаграмма самопроизвольного окисления. [5] |
Равновесные окислительно-восстановительные потенциалы двух разных окислителей различны. [6]
Из диаграммы видно, что смещение равновесного окислительно-восстановительного потенциала катодного деполяризатора ( окислителя) при сохранении остальных параметров постоянными будет повышать вероятность перехода системы из активного состояния в пассивное. [7]
Быстрое и обратимое протекание на электроде электрохимических реакций приводит к возникновению на нем равновесного окислительно-восстановительного потенциала. [8]
Условие термодинамической возможности электрохимической коррозии можно выразить как требование присутствия в электролите вещества - деполяризатора, равновесный окислительно-восстановительный потенциал которого более положителен, чем у корродирующего металла. [9]
Рассматривая рис. 151, легко понять, что скорость окисления металла должна зависеть от разности между равновесным окислительно-восстановительным потенциалом окислителя ( в нашем примере Ф вн) и равновесным потенциалом окисляемого металла Ф аевн. [10]
Все это, на наш взгляд, не позволяет отождествлять потенциалы перехода окраски 4 - СДФА с равновесными окислительно-восстановительными потенциалами. [11]
Из изложенного должно быть видно, что при описанном механизме равновесный потенциал перехода низшего окисла в высший - это такая же переменная величина, как, скажем, равновесный окислительно-восстановительный потенциал системы Fe2 / Fe3 в растворе. [12]
В отличие от ионно-металлических электродов, где металл и раствор обмениваются катионами, в окислительно-восстановительных ( О - В) электродах между этими фазами осуществляется электронный обмен. Для установления равновесного окислительно-восстановительного потенциала необходимо прежде всего, чтобы ионы металлов не переходили через границу фаз. [13]
Все обратимые окислительно-восстановительные процессы характеризуются равновесным потенциалом. В общей форме равновесный окислительно-восстановительный потенциал определяют по уравнению Нернста. [14]
На рис. 13 приведена диаграмма, показывающая установление коррозионного потенциала для полностью поляризованного сплава. В отличие от диаграммы Эванса за начальное положение анодных кривых принимается равновесный потенциал каждой структурной еоетавляющей и физически неоднородного участка металла и равновесный окислительно-восстановительный потенциал среды. [15]
Страницы: 1 2