Ионизационный потенциал - молекула
Cтраница 2
Ионизационный потенциал молекулы HF равен 15 8 в. По отношению к нагреванию фтористый водород очень устойчив: его термическая диссоциация становится заметной лишь около 3500 С. [16]
Ионизационный потенциал молекулы этана равен 11 7 в, а эффективный радиус метильной группы - - 1 77 А. [17]
Современный метод предполагает знание: а) ионизационного потенциала молекулы, б) кристаллической структуры и в) главных молекулярных поляризуемостей. Проведено сравнение величин энергий удаления электрона из индивидуальной молекулы и из молекулы в кристалле с известной структурой. Разность Р обусловлена взаимодействием положительно заряженных центров с окружающими их зарядами. Положительный заряд сосредоточен на участке молекулы ( точечное приближение) и поляризует молекулы кристалла в степени, зависящей от их ориентации и составляющих поляризуемости. Затем вычисляют вторичный эффект взаимодействия поляризованных молекул с их окружением. Как можно видеть из табл. 5, наблюдается значительно лучшее совпадение теоретических и экспериментальных данных, чем можно было бы ожидать. [18]
А и / в - приблизительно равны ионизационным потенциалам молекул. Поэтому ясно, что такое взаимодействие будет лишь незначительно изменять межплоскостные расстояния. [19]
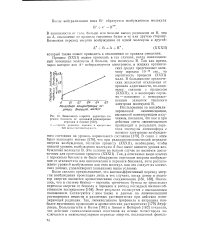 |
Зависимость скорости радиолиза перекиси бензоила от начальной концентрации. [20] |
Процесс ( XXXI) может протекать в тех случаях, когда ионизационный потенциал молекулы А больше, чем молекулы В. Так как время, через которое ион А нейтрализуется электроном, в жидких органических средах представляет величину порядка 10 13 сек. [21]
Существуют некоторые указания на то, что введение з амести-теля, который уменьшает ионизационный потенциал молекул, увеличивает интенсивность линий молекулярного иона в масс-спектре. [22]
Подобное же уравнение ( с поправкой на характеристику прибора) служит для расчета ионизационных потенциалов молекул, определяемых с помощью фотоэлектронной спектроскопии. Ультрафиолетовое излучение вызывает испускание электронов, принадлежащих валентным оболочкам молекул, и может быть использовано при определении их ионизационных потенциалов. [23]
Выражение ( 73) следует из теории дисперсионных сил Лондона при условии равенства ионизационных потенциалов молекул смеси. [24]
Количество энергии, необходимое для превращения нейтральной молекулы в положительный ион, называется ионизационным потенциалом молекулы. [25]
 |
Процессы ионной рекомбинации. Схема электронного захвата в гетерогенной полимерной смеси вблизи межфазной границы домена. [26] |
Легко показать, что большая часть вторичных электронов имеет энергию ниже уровня, соответствующего обычным ионизационным потенциалам молекул, и следовательно, длина их свободного пробега в полимерах при плотности около единицы должна составлять лишь несколько ангстрем. Однако небольшая часть электронов может обладать энергией больше нескольких сотен электронвольт. [27]
С увеличением длины сопряженной цепи максимум поглощения в ультрафиолетовой области спектра сдвигается в сторону длинных волн: ионизационные потенциалы молекул уменьшаются. [28]
Для силовых констант связей даются значения 9 8 ( С С) и 16 5 ( С О), а для ионизационного потенциала молекулы - 10 8 в. На воздухе она горит синим пламенем с выделением копоти, а при взаимодействии с водой дает малоновую кислоту. [29]
Более детальная расшифровка зависимостей / - / ( Z) затруднена вследствие одновременного влияния на / самых различных факторов. Ионизационные потенциалы молекул того же порядка, что и для атомов, и меняются обычно в пределах 54 - 15 В. [30]
Страницы: 1 2 3 4