Электродный потенциал - цинк
Cтраница 3
Кадмий применяют в процессах кадмирования аналогично тому, как цинк - в процессах цинкования. Поскольку электродный потенциал кадмия положительнее электродного потенциала цинка, кадмированные поверхности железных ( стальных) деталей более стойки по отношению к агрессивным средам. Такие детали используются в автомобилях, самолетах и др. В металлургических процессах кадмий идет для получения легкоплавких сплавов. Важной в технике является кадмиевая бронза ( - 1 % Cd), из которой делают телеграфные, телефонные, троллейбусные провода, поскольку кадмиевая бронза характеризуется большей прочностью и износостойкостью, чем медь. Кадмий используется в щелочных аккумуляторах. Чрезвычайно интересна способность Cd поглощать медленные нейтроны, вследствие чего он применяется в ядерных реакторах для регулирования скорости распада ядерного топлива. [31]
Цинк как самостоятельный конструкционный материал находит крайне ограниченное применение, так как по совокупности механических свойств и химической стойкости он не превосходит стали, но значительно дороже. В связи с тем, что электродный потенциал цинка отрицательнее, чем основных конструкционных металлов, его используют в качестве материала для протекторов. [32]
Процесс восстановления ионов железа, никеля и меди в данных условиях будет самопроизвольным процессом, если он сопровождается окислением цинка. Это требование эквивалентно тому, что электродный потенциал цинка должен быть более отрицательным по отношению ко всем остальным. Такое соотношение действительно имеет место. Следовательно, цинк может восстановить в данных условиях все перечисленные выше ионы. [33]
Цинк как самостоятельный конструкционный материал находит крайне ограниченное применение, так как по совокупности механических свойств и химической стойкости он не превосходит стали, но значительно дороже. В связи с тем, что электродный потенциал цинка отрицательнее, чем основных конструкционных металлов, его используют в качестве материала для протекторов. [34]
Для защиты от коррозии насосно-компрессорных труб используют цинк. Сравнительно небольшая стоимость, а главное, более отрицательный электродный потенциал цинка ( - 0 76 В) обусловливает его применимость для защиты крупногабаритных конструкций. Цинк в среде водных электролитов является по отношению к железу анодом, и, медленно растворяясь, предохраняет железо или сталь от коррозии. [35]
 |
Стандартные электрохимические потенциалы некоторых элементов при 25 С по отношению к стандартному водородному электроду. [36] |
Напряжение гальванического элемента может изменяться в зависимости от концентрации находящегося в нем электролита. Например, изменяя концентрацию ионов цинка в цинковом полуэлементе, мы сместим, согласно принципу Ле Ша-телье, равновесие между цинком и ионами цинка, и вследствие этого изменится электродный потенциал цинка. При [ Zn2 ] 1 моль / л стандартный потенциал этого электрода равен 0 76 В, но при уменьшении [ Zn2 ] равновесие Zn Zn2 2e - смещается в правую сторону, а поскольку электродный потенциал является мерой способности реакции к самопроизвольному протеканию, ясно, что в данной ситуации он должен возрасти. [37]
 |
Схема перехода от обычного гальванического элемента к микроэлементам. [38] |
Рассмотрим, например, случай коррозии цинка, загрязненного медью. Так как растворимость меди в цинке ограничена, то при содержании меди в цинке выше определенного процента м едь выделяется в виде отдельных мелких включений. Электродный потенциал меди значительно выше электродного потенциала цинка, и, следовательно, цинк должен переходить в раствор электролита, а на меди должен выделяться водород. Включения меди в цинке очень малы и их трудно об - наружить невооруженным гла - зом. [39]
 |
Двойной электрический слой на границе раздела металл - раствор. [40] |
Рассмотрим систему, в которой два электрода находятся в растворах собственных ионов. Для предотвращения прямого взаимодействия окислителя и восстановителя электроды отделены друг от друга пористой перегородкой. В результате протекания этого процесса возникает электродный потенциал цинка. В результате возникает электродный потенциал меди. [41]
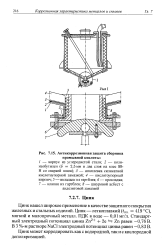 |
Антикоррозионная защита сборника промывной кислоты. [42] |
Стандартный электродный потенциал цинка Zn2 2е Zn равен - 0 76 В. В 3 % - м растворе NaCl электродный потенциал цинка равен - 0 83 В. [43]
 |
Двойной электрический слой на границе раздела металл - раствор. [44] |
Рассмотрим систему, в которой два электрода находятся в растворах собственных ионов. Примером может служить гальванический элемент Даниэля - Якоби, схема которого приведена на рис. VII. Для предотвращения прямого взаимодействия окислителя и восстановителя электроды отделены друг от друга пористой перегородкой. В результате протекания этого процесса возникает электродный потенциал цинка. На поверхности медной пластины также возникает двойной электрический слой и устанавливается равновесие CustCu2 2e - поэтому возникает электродный потенциал меди. [45]
Страницы: 1 2 3 4