Замена - анион
Cтраница 1
Замена анионов, находящихся во внешней сфере комплексного соединения, другими ионами ( например, замена хлор-иона бром-ионом или сульфат-ионом) производится без особых затруднений. С целью такой замены действуют на раствор комплексного аммиаката большим избытком какой-либо соли, содержащей нужный анион и такой катион, который образует нерастворимую соль с анионом внешней сферы комплексного соединения. [1]
Замена аниона в таллийорганических соединениях производится обычными путями, принятыми при работе с устойчивыми металлоорганическими солями. [2]
Замена тетра-фенилборатного аниона в соединении LXVI на бром-анион приводит к веществу, лишенному фотохромных свойств. [3]
Замена аниона соли также сказывается на формах гидроксокомплексов и константах гидролиза. Изменение форм вызвано взаимодействием анионов с ионами металла ( конкурирующее комплексообразование) или с растворителем. Так, сульфат-ион, образуя комплексы с ионом никеля, уменьшает степень полимеризации. Следовательно, меняя исходную соль ( хлорид, нитрат, сульфат), можно получить различающиеся по вязкости и адгезионным свойствам клеи. [4]
После замены обменных анионов анионами растворенных в воде электролитов анионит истощается и теряет способность обменивать ионы. [5]
При этом происходит замена аниона бензол ( толуол) - сульфата ионом хлора и омыление ацетильных групп. [6]
Анионирование воды ведется в целях замены удаляемых анионов на ион гидрокеила. При сочетании ОН-анионирования с Н - ка-тионированием происходит удаление из воды как анионов, так и катионов в обмен на ионы ОН иН, т.е. осуществляется химическое ( ионитное) обессоливание воды. [7]
Однако, как отмечалось нами выше, замена аниона также приводит к изменению A. [8]
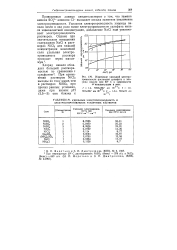 |
Изменение удельной электропроводности растворов сульфата и хлорида никеля при 60 С в зависимости от концентрации в итак. [9] |
Приведенные данные свидетельствуют о том, что замена аниона SO - анионом С1 - вызывает весьма заметное увеличение электропроводности. Удельная электропроводность хлорида никеля почти в два раза выше электропроводности сульфата никеля экаивалентной концентрации, добавление NaCl еще увеличивает электропроводность растворов. [10]
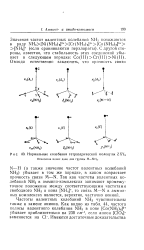 |
Нормальные колебания тетраэдрической молекулы ZXY3. [11] |
Частоты валентных колебаний NH3 чувствительны также к замене аниона. [12]
Бромистая циклопентадиенилртуть может быть получена из C5H5HgCl заменой аниона. При добавлении эквимолярных количеств галогенводородных кислот к раствору C5H5HgOH наблюдается реакция обмена аниона, в избытке кислоты происходит протолиз. Дициклопентадиенилртуть и циклопентадиенилмеркургалогениды не гидроли-зуются водой. [13]
Для выяснения, не связано ли изменение каталитической активности хинина при замене анионов индифферентного электролита с изменением его кислотно-основных свойств, были определены величины рКл первой ( более кислой) ступени ионизации хинина в 0 2 N растворах солей калия с различными анионами. На рис. 34 приведена зависимость lginp и Еп / 2 каталитической волны в 0 2 N растворах различных солей калия ( и 0 057V H2S04) от рКл хинина в тех же растворах солей. Из этого рисунка следует, что основной причиной изменения реакционной способности хинина под влиянием различных солей действительно является изменение его рКА вследствие образования ионных пар или комплексов ( по одной или обеим аминогруппам хинина) с анионами индифферентного электролита. C N03, который не совпадает с последовательностью анионов, усиливающих каталитическую активность хинина. Однако увеличение предельного тока в присутствии нитрата ( и в несколько меньшей степени - сульфата) и отклонение соответствующих точек вверх от прямой 1 на рис. 34 можно объяснить увеличением адсорбируемое хинина. Значительное же смещение Еи / 2 к отрицательным потенциалам в растворе сульфата объяснено [242] затруднением разряда комплекса хинина с дву-зарядным анионом SOl, имеющим, очевидно, менее положительный заряд, чем подобные комплексы с однозарядными анионами. [14]
При замене лиганда - использовании вместо 4-метилпири-дина 4 4 -дипиридила - или при замене тиоцианатного аниона формиатным можно селективно выделять о-ксилол. [15]
Страницы: 1 2 3