Изобарно-изотермический потенциал
Cтраница 2
Изобарно-изотермическим потенциалом G называется характеристическая функция состояния системы, убыль которой в обратимом процессе при постоянных давлении Р и температуре Т равна максимальной полезной работе. [16]
Почему изобарно-изотермический потенциал может рассматриваться как критерий при оценке направления самопроизвольно протекающей химической реакции. [17]
Рассмотрим изобарно-изотермический потенциал как критерий равновесия при изобарно-изотермическом процессе. [18]
Вычислить изобарно-изотермический потенциал рпар для 1 кг двуокиси углерода при 0 С и сравнить его значение со значением фжидк кипящей жидкости при этой же температуре. [19]
Оценить изобарно-изотермический потенциал полимеризации бутадиена-1 3 в полибутадиен, если мономер находится в жидком состоянии, а полимер - в аморфном твердом состоянии. [20]
Изменение изобарно-изотермического потенциала зависит не только от температуры, но и от относительных количеств веществ, участвующих в химической реакции, что будет более подробно рассмотрено далее. [21]
Изменение изобарно-изотермического потенциала в реакции зависит от относительных количеств веществ, взятых для осуществления химического процесса. [22]
Изменение изобарно-изотермического потенциала равно разности между изменениями его для конечных продуктов реакции и исходных реагентов. [23]
Изменение изобарно-изотермического потенциала AG либо рассчитывают, либо определяют на основе экспериментальных данных. [24]
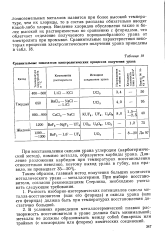 |
Сравнительные показатели электролитических процессов получения урана. [25] |
Разность изобарно-изотермических потенциалов окисла металла-восстановителя ( или его фторида) и окисла урана ( или его фторида) должна быть при температурах восстановления достаточно большой. [26]
Как изменяется изобарно-изотермический потенциал химической реакции по мере приближения системы к состоянию равновесия. [27]
При равновесии изобарно-изотермические потенциалы чистого вещества G, и этого же вещества в растворе Gt равны друг другу. [28]
Это уменьшение изобарно-изотермического потенциала достигает определенного равновесного значения в процессе растворения, после чего он уже не изменяется со временем. [29]
Определяя изменение изобарно-изотермического потенциала ( энергии Гиббса) для реакций, которые протекают в рассматриваемом процессе, и сравнивая их, устанавливают термодинамически наиболее вероятную реакцию. [30]
Страницы: 1 2 3 4