Замена - концентрация
Cтраница 1
Замена концентраций на активности позволяет по уравнению изотермы реакции получить выражение для энергии реакции. Подсчет констант равновесия также следует проводить с заменой концентраций на активности. [1]
Замена концентраций активностями в выражении / Сд делает его применимым к растворам сильных электролитов и концентрированным растворам слабых электролитов. [2]
Замена концентрации компонента его активностью не вскрывает физической сущности неидеальности растворов, так как введение активности является чисто формальным приемом. [3]
При замене концентрации некоторой ее степенью имеют место следующие преобразования кривых свойства. [4]
Внесение поправок на неидеальность растворов ( замена концентраций активностями) позволяет применять для них закономерности, выявленные химической термодинамикой. [5]
Применение закона распределения Шилова к электролитам требует замены концентраций на активности. [6]
В разбавленном растворе uiCi, а при любых более высоких концентрациях закон Генри сохраняется при замене концентрации активностью. [7]
Универсальность уравнений термодинамики, описывающих равновесия для идеальных растворов, сохраняется, если в них произвести замену концентраций термодинамическими активностями. Активность - это такая функция от концентрации раствора, которая позволяет связать разные свойства раствора друг с другом без изменения простой формы соответствующих термодинамических уравнений. Таким же свойством обладает летучесть, которая заменяет давление в уравнениях теории растворов или газовых равновесий. [8]
В разбавленном растворе а, С -, при более высоких концентрациях закон Генри сохраняется при замене концентрации активностью. [9]
Ввиду того что все последующие стадии процесса предполагаются одинаковыми, выражение для скорости суммарной реакции отличается заменой концентрации молекулярного брома на интенсивность поглощенного света. [10]
Расчет летучести i - ro компонента в газовой фазе f r производится по той же формуле с заменой концентрации xt на у г, а коэффициенты смеси рассчитываются по составу газовой фазы. Расчет летучести ведется при задании начального приближения по составу обеих фаз. [11]
В разбавленном растворе а - - - С /, а при любых концентрациях закон Генри сохраняется при замене концентрации активностью. [12]
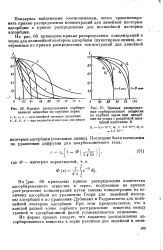
На [ рис. 69 приведены кривые распределения количества адсорбированного вещества в зерне, полученные из кривых расгределения концентраций путем замены концентрации на величину адсорбции по уравнению Генри для линейной изотермы адсорбции и по уравнению Дубинина и Радушкевича для нелинейной изотермы адсорбции. При этом предполагается, что в каждой данной точке сорбента распределение вещества между газовой и адсорбционной фазой устанавливается мгновенно. [14]
Уравнение ( 10) справедливо для всех водных систем, в которых находятся и другие протолиты, при условии замены концентрации на активности. Коэффициенты активности и в этом случае определяются через ионную силу раствора. Уже при ионной силе / 10 - 3 значения рН сильно изменяются, что необходимо учитывать при сравнении данных, полученных расчетом и из потенциометрических измерений. [15]
Страницы: 1 2 3