Замена - атом - углерод
Cтраница 1
Замена атома углерода на гетероатом азота в некоторой степени нарушает равномерность распределения электронной плотности, вследствие чего изменяются длины связей. [1]
Замена атома углерода на атом азота в 5-членном хелатном цикле приводит к образованию более устойчивых в кислых растворах хелатов. [2]
 |
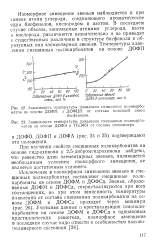
Уровни энергии несвязывающей ( л и нижней разрыхляющей ( я МО нечетных альтернантных систем. [3] |
При замене атома углерода более электроотрицательным ге-тероатомом ( например, атомом азота) энергии как несвязывающей, так и низшей разрыхляющей орбиталей снижаются, при замене менее электроотрицательным гетероатомом ( например, атомом мышьяка) - повышаются. Но это верно только в том случае, если коэффициент Сц ( - при данном атоме не равен нулю. В противном случае замена такого атома углерода гетероатомом не изменяет энергию несвязывающей орбитали и отражается лишь на энергии низшей разрыхляющей МО. [4]
О, и замена атомов углерода атомами кислорода в этом интервале составов уже существенно отражается на свойства. Вероятно, энергии связей Ti-С и Ti-О в оксикарбидах титана близки, а связей Zr-С и Zr-О в оксикарбидах циркония отличаются. [5]
В отдельных случаях возможна замена атома углерода, общего для трех циклов. [6]
Резко повышает теплостойкость полимера замена атомов углерода в основной цепи атомами кремния, титана, железа, олова, примером чего может служить синтез кремнийорганического каучука. [7]
Этот переход легко понять, поскольку замена атома углерода более электроотрицательным атомом второго периода, как правило, снижает энергию как занятых, так и свободных МО. [8]
Изоморфное замещение звеньев наблюдается и при замене атома углерода, соединяющего ароматические ядра бисфенолов, кислородом и азотом. В последнем случае объемы, занимаемые атомами углерода, азота и кислорода, различаются незначительно и не приводят к существенным различиям в структуре бисфенола и образуемых ими элементарных звеньев. [10]
Если кислотная функция построена ( формально) путем замены карбоксильного атома углерода на атом серы ( селена или теллура), то ставится полное название элемента. [11]
В соответствии с этим константа скорости даже несколько увеличивается при замене атома углерода на серу и уменьшается при замене одного, а затем и обоих атомов углерода на азотные. При замене атома углерода на кислород, реакционная способность кратной связи становится настолько малой, что наблюдать ее в в условиях опыта не удается. [12]
Метод Хюккеля направлен на получение качественных заключений о стабильности систем, о тенденциях в изменении энергии или других свойств, например распределения электронной плотности, при переходе от одного соединения к другому, в частности при переходе, определяемом заменой атома углерода на гетероатом либо изомеризацией. При этом, конечно, надо помнить о том, что меняется не только л-электронная структура задачи. Меняется и то, что связано с о-орбиталями, однако подчас эти изменения либо можно учесть в рамках того же разделения задач для о - и л-подсистем и после рассмотрения изменений в - электронной задаче добавить соответствующие поправки от осоставляющей, либо рассматривать такие ситуации, в которых изменение о-подсистемы малосущественно и им можно пренебречь, например при расчетах энергий первых л-электронных переходов в родственных системах и качественном сопоставлении получаемых величин. [13]
В соответствии с этим константа скорости даже несколько увеличивается при замене атома углерода на серу и уменьшается при замене одного, а затем и обоих атомов углерода на азотные. При замене атома углерода на кислород, реакционная способность кратной связи становится настолько малой, что наблюдать ее в в условиях опыта не удается. [14]
Энтальпия специфического взаимодействия полициклоаре-нов с N-метилпирролидоном возрастает с увеличением числа конденсированных циклов на 10 - 15 кДж / моль. При замене атома углерода в молекуле полициклоарена ( например, флуорена) на атом кислорода энтальпия специфического взаимодействия с N-метилпирролидоном повышается на 5.7 кДж / моль, а при замене на группу N - Н - на 22.7 кДж / моль. Такое значительное усиление специфических взаимодействий с карбазолом обусловлено дополнительным к образованию л-комплексов существованием водородных связей с N-метилпирролидоном. [15]
Страницы: 1 2