Замена - алкильный радикал
Cтраница 2
Сравнение данных по энергиям связей арилтриалкил - и диарилдиал-килсиланов показывает, что замена алкильного радикала на арильный приводит к значительному увеличению энергии связи. Особенно резко возрастают энергии связей при переходе от 3 4-диметилфенилтриалкилси-ланов к соответствующим ди - ( 3 4-диметилфенил) диалкилсиланам. [16]
Изменение сольватного числа, по-видимому, обусловлено изменением стереохимии фосфорорганической кислоты при замене алкильного радикала в молекуле фосфиновой кислоты на фенильный. [17]
 |
Инфракрасный спектр ( СН3 СвН581 [ СН2СН2СНг8ЦСвНв з ] г. [18] |
При изучении реакции присоединения гидридсиланов к аллилпроизводным кремния установлено, что активность двойной связи в моно-и диаллилпроизводных кремния зависит от природы атомов и групп, связанных с атомом кремния. При замене алкильных радикалов в триал-килаллил - и диалкилдиаллилсиланах на заместители электроотрицательного характера ( атом хлора, фенильный радикал) двойная связь в ал-лильном радикале становится более активной. [19]
 |
Полярографические кривые восстановления эфиров тиосульфокислот. / - фон ( С2Н6 4 NI. [20] |
I), ( II) - алкан-и арентиосульфокислот составляет примерно - 1 4 - ( - 1 5) в насыщ. Таким образом, даже при замене алкильного радикала на арильный со стороны окисленной серы потенциал восстановления эфиров остается, практически, без изменения ( ЕЧ, - - 1 5 в насыщ. [21]
 |
Полярографические кривые восстановления эфиров тиосульфокислот. / - фон ( С2Н6 4 N1. [22] |
Для эфиров тиосульфокислот более характерной является вторая полярографическая волна, Еч, которой для алкилэфиров ( I), ( II) - алкан-и арентиосульфокислот составляет примерно - 1 4 - ( - 1 5) в насыщ. Таким образом, даже при замене алкильного радикала на арильный со стороны окисленной серы потенциал восстановления эфиров остается, практически, без изменения ( Ечг - 1 5 в насыщ. [23]
Природа спиртового радикала мало влияет на скорость гидролиза. Некоторое увеличение скорости гидролиза наблюдается при удлинении или разветвлении цепочки спиртовой молекулы, а также при переходе от первичного спирта ко вторичному. Замена алкильного радикала на алициклический не влияет на характер гидролиза. [24]
Таким образом, из изученных нами реакций взаимодействия гидрид-силанов с аллилпроизводными кремния видно, что активность двойной связи в моно - и диаллилпроизводных кремния в реакциях присоединения гидридсиланов зависит от природы атомов и групп, связанных с атомом кремния. С ростом органических радикалов с прямой цепью в триалкилал-лил - и диалкилдиаллилсиланах активность двойной связи у аллильного радикала увеличивается. При замене алкильных радикалов в триалкилал-лил - и диалкилдиаллилсиланах на заместители электроотрицательного характера ( фенильный радикал или атом хлора) двойная связь в аллиль-ном радикале становится еще более активной. [25]
Эфиры фосфорной кислоты не отличаются хорошими вязкостно-температурными свойствами. Последовательное замещение алкильных групп арильными приводит к повышению вязкости и уменьшению индекса вязкости. Последнее наблюдается и при замене нормальных алкильных радикалов разветвленными. [26]
Из табл. 24 видно, что наибольшей растворяющей способностью по отношению к воде обладают ароматические углеводороды и прежде всего бензол. Растворимость воды в ароматических углеводородах определяется их молекулярным весом. С увеличением последнего растворимость воды довольно резко снижается. Замена алкильного радикала в ароматическом ядре на пятичленный циклоалкильный не оказывает существенного влияния на растворимость воды. [27]
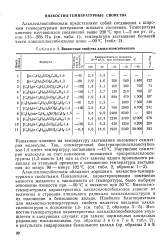 |
Вязкостные свойства алкилсилоксибензолов. [28] |
Алкилсилоксибензолы обладают хорошими вязкостно-температурными свойствами. Показателем, характеризующим изменение вязкости жидкости в зависимости от температуры, было выбрано отношение вязкости при - 50 С к вязкости при 50 С. Вязкостно-температурная характеристика алкилсилоксибензолов зависит от величины и строения алкильного радикала алкилсилоксигрупп и их положения в бензольном кольце. Вязкостно-температурная характеристика алкилсилоксибензолов ухудшается в следующих случаях: при замене нормальных алкильных радикалов изоалкильными ( ср. [29]
С целью изучения влияния строения углеводородного радикала на противоизносную - и противокоррозионную эффективность производных ДТФ кислот синтезированы некоторые их алкиловые и аллиловые эфиры [ 45, с. Установлена определенная зависимость противозадирного действия от длины и характера алкиль-ного радикала в эфирах ДТФ кислот. Наивысшей противозадир-ной эффективностью обладают S-аллиловые эфиры О О-диизопро-пилдитиофосфорной кислоты. С увеличением длины О-алкильного радикала в дитиофосфорной группе эффективность их ухудшается, а увеличение длины S-алкильного радикала не оказывает заметного влияния. Замена алкильного радикала на аллильный приводит к некоторому повышению противозадирных свойств; особенно заметно повышение нагрузки сваривания. [30]
Страницы: 1 2 3